��Ŀ����
Ǧ��һ���ؽ��������ԭ������Ϊ207��Ǧ��Ǧ�Ļ������кܶ���;�������صȣ���Ǧ��������ж���ȼú��������ұ�����ȶ�����Ҫ��Ǧ��ȾԴ��Ǧһ������������ۻ��������ԡ��������Ѫ��������Ϊ���˽���е�Ǧ��Ⱦ���⣬С�������ͬѧ�ǽ��������µ��о���
��1��С����ĵ����ϣ�ͼ�м�¼����ij��·��ͬ���봦��ֲ�ľ��IJ���Ǧ�ĺ�����ͬ���ɴ��Ʋ⣺���IJ���ҶƬ��Ǧ����ֱ������ ����ɾ��IJ���ΧҶƬ��Ǧ����ͬ����Ҫԭ�� ������˵������ԭ��
��2�����Ķ�����ʱ��С���ַ��֣���ͯ�ӿ����������Ǧ���dz�����������1.6��1.7����Ϊ��̽�����������չ�������µ��о���������ѧ֪ʶ���������գ�
�ٿ�������Ϊ��
��ͨ��ȡ���������õ���һ��ʵ�����ݣ�
��������ʵ�����ݣ����Եó��Ľ���� ��ɴ˽����ԭ�������
��3�����߷õ����У�С��۲쵽ij�������ϳ��ų��ķ�ˮ������ɫ������������Ǧ��Ϊ�˲ⶨ��ˮ��Ǧ��Ũ�ȣ������������ʵ�鲽�裺
��ˮ��Ʒ
��Pb2+��Һ
��PbCrO4��Һ
�ٲ����й�����Ҫ�IJ��������� �� �Ͳ�������
�ڲ�����a������Ϊ ��ȱ�ٴ˲�������ý�� ���ƫ�ߡ�����ƫ�͡�������Ӱ�족����
��4��ͨ���о���С�������һϵ�н���Ǧ�Ի�����Ⱦ�Ľ��飬���н����в�ǡ������
A������ֹͣʹ�ú�Ǧ����
B�������µ���Ǧȼ��
C������ʹ��Ǧ�����������ĵ綯��
D��ȼú�糧������ұ�����ķ������������ŷţ�
��1��С����ĵ����ϣ�ͼ�м�¼����ij��·��ͬ���봦��ֲ�ľ��IJ���Ǧ�ĺ�����ͬ���ɴ��Ʋ⣺���IJ���ҶƬ��Ǧ����ֱ������
��2�����Ķ�����ʱ��С���ַ��֣���ͯ�ӿ����������Ǧ���dz�����������1.6��1.7����Ϊ��̽�����������չ�������µ��о���������ѧ֪ʶ���������գ�
�ٿ�������Ϊ��
��ͨ��ȡ���������õ���һ��ʵ�����ݣ�
| �����߶ȣ�m�� | 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 2.0 |
| Ǧ��Ũ�ȣ�ug/m3�� | 1.10 | 0.98 | 0.91 | 0.72 | 0.66 | 0.54 | 0.50 |
��3�����߷õ����У�С��۲쵽ij�������ϳ��ų��ķ�ˮ������ɫ������������Ǧ��Ϊ�˲ⶨ��ˮ��Ǧ��Ũ�ȣ������������ʵ�鲽�裺
��ˮ��Ʒ
| ��ѧ���� |
| K2CrO4 |
| ���� |
| ϴ�� |
| a |
| ���� |
�ٲ����й�����Ҫ�IJ���������
�ڲ�����a������Ϊ
��4��ͨ���о���С�������һϵ�н���Ǧ�Ի�����Ⱦ�Ľ��飬���н����в�ǡ������
A������ֹͣʹ�ú�Ǧ����
B�������µ���Ǧȼ��
C������ʹ��Ǧ�����������ĵ綯��
D��ȼú�糧������ұ�����ķ������������ŷţ�
���㣺���������������Ⱦ������
ר�⣺Ԫ�ؼ��仯����,��ѧӦ��
��������1����·����ʻ�������ŷŵ�β������Ǧ������Χ�����������IJ˸�ϸ�����������Σ���ͬ����Ǧ��Ⱦ�����ͬ��
��2���ٸ���������ͼ�����֣�������Ϣ���ɵó�����һ���������治ͬ�߶ȵĿ�����Ǧ����ͬ���о����ݣ�
����������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ�Ǧ��Ǧ�������ܶȴ�
��3���ٸ���ʵ�����ѡ�������������
��ʵ�������������˲�������Գ���ǰӦ�����˵IJ������ɣ����������������ƫ��
��4���ܹ������ų���Ǧ������Ľ��鲻ǡ����
��2���ٸ���������ͼ�����֣�������Ϣ���ɵó�����һ���������治ͬ�߶ȵĿ�����Ǧ����ͬ���о����ݣ�
����������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ�Ǧ��Ǧ�������ܶȴ�
��3���ٸ���ʵ�����ѡ�������������
��ʵ�������������˲�������Գ���ǰӦ�����˵IJ������ɣ����������������ƫ��
��4���ܹ������ų���Ǧ������Ľ��鲻ǡ����
���
�⣺��1����·����ʻ�������ŷŵ�β������Ǧ������Χ�����������IJ˸�ϵ��������뵽��������Ӫ�����ʣ���˾��IJ���ҶƬ��Ǧ����ֱ��������������ϵ���գ�����ɾ��IJ���ΧҶƬ��Ǧ����ͬ����Ҫԭ��������β����Ǧ���빫·���벻ͬ�������к�Ǧ����ͬ����ȼú��������ұ�����ȣ�
�ʴ�Ϊ����������ϵ���գ�������β����Ǧ���빫·���벻ͬ�������к�Ǧ����ͬ����ȼú��������ұ�����ȣ�
��2������������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ����Եó��Ľ���������Խ�ͣ���Ǧ��Խ�ߣ���֪��������ӦΪ�����治ͬ�߶ȿ�����Ǧ�����о���
�ʴ�Ϊ�������治ͬ�߶ȿ�����Ǧ�����о���
����������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ���Ϊ�����Խ�ͣ���Ǧ��Խ�ߣ�˵��Ǧ��Ǧ�������ܶȴ�
�ʴ�Ϊ�������Խ�ͣ��ߣ�����Ǧ��Խ�ߣ��ͣ��� Ǧ��Ǧ�������ܶȴ�
��3������ʵ�鲽���֪�������ձ��д�����ˮ������ˮ�е�Ǧת��Ϊ�����������й��ˣ�ϴ�Ӻ�ɣ�������Ǧ���������貣���������ձ���©������������
�ʴ�Ϊ���ձ���©����
��ʵ��������������ϴ�Ӻ�������Գ���ǰӦ������ϴ�Ӻ�IJ������ɣ�����Ǧ�������������ƫ��÷�ˮ��Ǧ�ĺ���ƫ�ߣ�
�ʴ�Ϊ����ɣ�ƫ�ߣ�
��4��A����������ֹͣʹ�ú�Ǧ���ͣ�Ӯʹ����Ǧ���ͣ����Լ���β���к�Ǧ�������ŷţ���A����
B�������µ���Ǧȼ�ϣ����Լ���ȼ�պ�Ǧ�������ʵ��ŷţ���B��ȷ��
C��Ǧ��������Ǧ������Ǧ���缫�������ĵ�ػ���ɶԻ�������Ⱦ����C����
D��ȼú�糧������ұ�����ķ������������ŷţ����Լ��ٷ�����Ǧ�ĺ�������D��ȷ��
��ѡAC��
�ʴ�Ϊ����������ϵ���գ�������β����Ǧ���빫·���벻ͬ�������к�Ǧ����ͬ����ȼú��������ұ�����ȣ�
��2������������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ����Եó��Ľ���������Խ�ͣ���Ǧ��Խ�ߣ���֪��������ӦΪ�����治ͬ�߶ȿ�����Ǧ�����о���
�ʴ�Ϊ�������治ͬ�߶ȿ�����Ǧ�����о���
����������ͼ����֪�������߶�Խ�ߣ�������Ǧ��Խ�ͣ���Ϊ�����Խ�ͣ���Ǧ��Խ�ߣ�˵��Ǧ��Ǧ�������ܶȴ�
�ʴ�Ϊ�������Խ�ͣ��ߣ�����Ǧ��Խ�ߣ��ͣ��� Ǧ��Ǧ�������ܶȴ�
��3������ʵ�鲽���֪�������ձ��д�����ˮ������ˮ�е�Ǧת��Ϊ�����������й��ˣ�ϴ�Ӻ�ɣ�������Ǧ���������貣���������ձ���©������������
�ʴ�Ϊ���ձ���©����
��ʵ��������������ϴ�Ӻ�������Գ���ǰӦ������ϴ�Ӻ�IJ������ɣ�����Ǧ�������������ƫ��÷�ˮ��Ǧ�ĺ���ƫ�ߣ�
�ʴ�Ϊ����ɣ�ƫ�ߣ�
��4��A����������ֹͣʹ�ú�Ǧ���ͣ�Ӯʹ����Ǧ���ͣ����Լ���β���к�Ǧ�������ŷţ���A����
B�������µ���Ǧȼ�ϣ����Լ���ȼ�պ�Ǧ�������ʵ��ŷţ���B��ȷ��
C��Ǧ��������Ǧ������Ǧ���缫�������ĵ�ػ���ɶԻ�������Ⱦ����C����
D��ȼú�糧������ұ�����ķ������������ŷţ����Լ��ٷ�����Ǧ�ĺ�������D��ȷ��
��ѡAC��
���������⿼��̽����ʵ�顢ɸѡ��Ϣ��������ʵ�鷽��������ȣ���Ŀ�Ѷ��еȣ��ۺ��Խϴ��Ƕ�ѧ���ۺ��������飮��ѧ��ȫ�����ջ���֪ʶ��

��ϰ��ϵ�д�
 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
�����Ŀ
�ڲ�ͬ�¶��µ�ˮ��Һ������Ũ��������ͼ��ʾ������˵������ȷ���ǣ�������
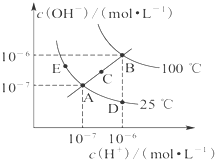

| A��ͼ�����KW��Ĺ�ϵ��B��C��A=D=E |
| B��AB���ϵĵ�һ����������Һ |
| C��D������Ǵ�����Һ��E������Ǵ�������Һ |
| D����E����Һ��ˮϡ�Ϳ��ܱ�ΪD�� |
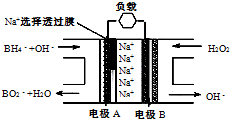 ֱ��NaBH4/H2O2ȼ�ϵ�أ�DBFC���Ľṹ����ͼ���йظõ�ص�˵����ȷ���ǣ�������
ֱ��NaBH4/H2O2ȼ�ϵ�أ�DBFC���Ľṹ����ͼ���йظõ�ص�˵����ȷ���ǣ�������| A���缫B�����а���MnO2�㣬MnO2��������� |
| B����ظ������ĵ缫��ӦΪ��BH4-+8OH-+8e-=BO2-+6H2O |
| C���ŵ�����У�Na+ ������������Ǩ�� |
| D���ڵ�ط�Ӧ�У�ÿ����1L 6 mol/LH2O2��Һ��������������·�еĵ���Ϊ6NA�� |
����˵������ȷ���ǣ�������
�ٻ�ѧ��Ӧ��ʵ���ǻ�����к���ȡ��ʱ����Ч��ײ
����ͨ���Ӽ����ײ��ʱҲ�ܷ�����ѧ��Ӧ
�ۻ���ӱ���ͨ���Ӿ��нϸߵ�����
�ܻ�ѧ��Ӧ��ʵ����ԭ�ӵ��������
�ݻ�ѧ��Ӧ��ʵ���Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɹ���
����Ӽ����ײһ���ܷ�����ѧ��Ӧ��
�ٻ�ѧ��Ӧ��ʵ���ǻ�����к���ȡ��ʱ����Ч��ײ
����ͨ���Ӽ����ײ��ʱҲ�ܷ�����ѧ��Ӧ
�ۻ���ӱ���ͨ���Ӿ��нϸߵ�����
�ܻ�ѧ��Ӧ��ʵ����ԭ�ӵ��������
�ݻ�ѧ��Ӧ��ʵ���Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɹ���
����Ӽ����ײһ���ܷ�����ѧ��Ӧ��
| A���٢ۢܢ� | B���ڢۢ� |
| C���ۢܢݢ� | D���ڢܢ� |
����Ƥा�������������Ч����Ƥ�ؾ��п������˾������ã�������һ������������ͼ��ʾ��ת����ϵ�������й�˵����ȷ���ǣ�������
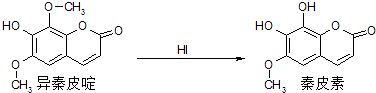

| A������Ƥष���ʽΪC11H14O5 |
| B������Ƥ�����Ƥ�ؾ�����NaHCO3��Һ��Ӧ���ų�CO2 |
| C������Ƥ�����Ƥ�ؿ���FeCl3��Һ���� |
| D��1mol����Ƥ��������4mol NaOH��Ӧ |
 ��Ի�ѧ��Ӧ�е������仯����������⣮
��Ի�ѧ��Ӧ�е������仯����������⣮