题目内容
已知钡的金属活动性处于钾和钠之间,下列反应可以实现的是( )
| A、钡可以从氯化钾溶液中置换出钾 |
| B、钡可以从冷水中置换出氢而得到氢气 |
| C、钡可以从氯化钠溶液中置换出钠 |
| D、在溶液加入金属锌可以观察到有钡析出 |
考点:常见金属的活动性顺序及其应用
专题:金属概论与碱元素
分析:钡的金属活动性处于钾和钠之间,所以Ba能和冷水反应生成氢气,Ba的金属性大于Zn,据此分析解答.
解答:
解:A.Ba的金属活动性介于K和Na之间,则Ba能和KCl溶液中的水反应生成氢氧化钡和氢气,且K的金属活动性大于Ba,所以不能置换出K,故A错误;
B.Ba的金属活动性介于K和Na之间,Na能和冷水反应生成NaOH和氢气,则Ba也能和冷水反应生成氢氧化钡和氢气,故B正确;
C.Ba能和水反应生成氢氧化钡和氢气,虽然Ba的金属活动性大于Na,但Ba不能从氯化钠溶液中置换出Na,故C错误;
D.金属活动性K>Ba>Na>Zn,且Ba能和水反应,所以锌不能置换出Ba,故D错误;
故选B.
B.Ba的金属活动性介于K和Na之间,Na能和冷水反应生成NaOH和氢气,则Ba也能和冷水反应生成氢氧化钡和氢气,故B正确;
C.Ba能和水反应生成氢氧化钡和氢气,虽然Ba的金属活动性大于Na,但Ba不能从氯化钠溶液中置换出Na,故C错误;
D.金属活动性K>Ba>Na>Zn,且Ba能和水反应,所以锌不能置换出Ba,故D错误;
故选B.
点评:本题考查了金属的性质,根据钠、钾的性质利用知识迁移法分析Ba的性质,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、1mol Cl2参加反应转移电子数一定为2NA |
| B、在反应KClO3+6HCl═KCl+3Cl2+3H2O中,每生成3mol Cl2转移电子数为6NA |
| C、SiO2与烧碱反应只生成盐和水,属于酸性氧化物 |
| D、Cl2的水溶液具有酸性,Cl2通入紫色石蕊溶液中,溶液只变红 |
下列物质中,属于强电解质的是( )
| A、Cu |
| B、H2O |
| C、H2SO4 |
| D、CH3COOH |
下列有关说法正确的是( )
| A、常温下,0.1mol?L-1 Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | ||
| B、常温下,0.1mol?L-1 HA溶液与0.1 mol?L-1 NaOH溶液正好完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) | ||
C、常温下,向0.1mol?L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中
| ||
| D、常温下,pH=7的CH3COONa和CH3COOH混合溶液中:c(Na+)=c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) |
下列过程属于化学变化的是( )
| A、煤的干馏 | B、蒸发 |
| C、萃取 | D、蒸馏 |
关于1mol?L-1的硫酸溶液的下列叙述中,不正确的是( )
| A、1L该溶液中含溶质98g |
| B、从10mL该溶液中取出5mL后,剩余溶液的浓度不变 |
| C、将4.9g浓硫酸加入盛有50mL蒸馏水的烧杯中充分溶解可配得该浓度的硫酸溶液 |
| D、该浓度的硫酸具有酸的通性,但不具有强氧化性 |
下列化学用语,应用正确的是( )
A、硝基苯的结构简式是: |
B、乙炔的电子式是: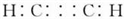 |
C、乙醚分子的球棍模型是: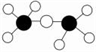 |
| D、甲酸中存在-CHO和-COOH两种官能团 |
下列反应中,属于加成反应的是( )
| A、甲烷与氯气混合,光照一段时间后黄绿色消失 |
| B、乙烯使酸性高锰酸钾溶液褪色 |
| C、将苯滴入少量到溴水中,振荡后水层接近无色 |
| D、乙烯使溴水褪色 |
把金属钠投入下列溶液中,有气体产生且溶液质量增加的是( )
| A、FeCl3溶液 |
| B、C2H5OH |
| C、饱和NaOH溶液 |
| D、CuSO4溶液 |