题目内容
下列实验中,不能达到预期目的是( )
| A、向某未知溶液中滴加足量稀盐酸,再加几滴BaCl2溶液,检验SO42-的存在 |
| B、用100mL量筒量取20.00mL Na2CO3溶液 |
| C、不用另加任何试剂就能鉴别HCl、Na2CO3、Na2SO4 和BaCl2四种无色溶液 |
| D、用粥汤检验淀粉溶液具有丁达尔效应 |
考点:化学实验方案的评价
专题:
分析:A.用盐酸酸化的BaCl2溶液检验SO42-的存在;
B.滴定管的感量是0.01mL;
C.氯化钡能和碳酸钠、硫酸钠生成白色沉淀,和HCl不反应,HCl、Na2CO3相互滴加顺序不同其反应现象不同;
D.淀粉溶液中分散质直径在1-100nm之间,属于胶体.
B.滴定管的感量是0.01mL;
C.氯化钡能和碳酸钠、硫酸钠生成白色沉淀,和HCl不反应,HCl、Na2CO3相互滴加顺序不同其反应现象不同;
D.淀粉溶液中分散质直径在1-100nm之间,属于胶体.
解答:
解:A.用盐酸酸化的BaCl2溶液检验SO42-的存在,HCl能除去其它离子的干扰,氯化钡和硫酸根离子反应生成难溶于盐酸的白色沉淀,所以能实现实验目的,故A不选;
B.滴定管的感量是0.01mL,100mL量筒的感量1mL,所以应该用碱式滴定管量取20.00mL Na2CO3溶液,故B选;
C.氯化钡能和碳酸钠、硫酸钠生成白色沉淀,和HCl不反应,HCl、Na2CO3相互滴加顺序不同其反应现象不同,所以可以不用另加任何试剂就能鉴别这几种溶液,故C不选;
D.淀粉溶液中分散质直径在1-100nm之间,属于胶体,胶体具有丁达尔效应,故D不选;
故选B.
B.滴定管的感量是0.01mL,100mL量筒的感量1mL,所以应该用碱式滴定管量取20.00mL Na2CO3溶液,故B选;
C.氯化钡能和碳酸钠、硫酸钠生成白色沉淀,和HCl不反应,HCl、Na2CO3相互滴加顺序不同其反应现象不同,所以可以不用另加任何试剂就能鉴别这几种溶液,故C不选;
D.淀粉溶液中分散质直径在1-100nm之间,属于胶体,胶体具有丁达尔效应,故D不选;
故选B.
点评:本题考查化学实验方案评价,涉及胶体性质、物质鉴别、仪器的使用、离子检验等知识点,综合性较强,明确物质性质是解本题关键,知道常见离子的检验方法,注意常见仪器的使用方法,易错选项是B.

练习册系列答案
相关题目
向饱和BaSO4 溶液中加水,下列叙述正确的是( )
| A、BaSO4 溶解度增大、Ksp不变 |
| B、BaSO4 溶解度、Ksp均增大 |
| C、BaSO4 溶解度不变、Ksp增大 |
| D、BaSO4 溶解度、Ksp均不变 |
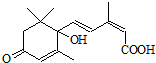 用S-诱抗素制剂,可以保证鲜花盛开.S-诱抗素的结构如图,则下列关于该物质的说法正确的是( )
用S-诱抗素制剂,可以保证鲜花盛开.S-诱抗素的结构如图,则下列关于该物质的说法正确的是( )| A、其分子中含有一个手性碳原子 |
| B、只能发生加聚反应,不能发生缩聚反应 |
| C、1 mol该物质与NaOH溶液反应,最多消耗2 mol NaOH |
| D、既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
下列从海水中提取镁正确的方法是( )(提示:熔点:MgO2 850℃MgCl2 714℃)
A、海水
| ||||||
B、海水
| ||||||
C、海水
| ||||||
D、海水
|
下列说法正确的是( )
| A、在新制的氯水中加入NaOH溶液至中性时,满足c(Na+)=c(ClO-)+c(HClO) |
| B、25℃时,稀释0.5 mol?L-1的NH4Cl溶液,水解平衡右移,水解平衡常数Kh增大,而Kw不变 |
| C、常温下,pH=11的某碱MOH溶液与pH=3的盐酸等体积混合后,溶液可能呈中性或酸性 |
| D、0.2mol?L-1CH3COOH溶液与0.1mol?L-1NaOH溶液等体积混合,则:2c(H+)-2c(OH)=C(CH3COO)-C(CH3COOH) |
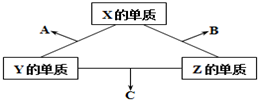 有X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化,已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数的少1个.请回答下列问题:
有X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图所示变化,已知一个B分子中含有Z元素的原子个数比一个C分子中含有Z元素的原子个数的少1个.请回答下列问题: