题目内容
Ⅰ.甲、乙、丙是三种不含相同离子的可溶性强电解质.它们所含离子如下表所示:
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙).(1)丙是 .
(2)甲是 ,设计实验确定甲的物质组成
(若乙物质组成确定,则此空不填).
Ⅱ.有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次增大.将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀.请回答下列问题:
(1)经检验,三种盐中还含有下列选项中的一种离子,该离子是 .
A.Na+ B.Mg2+ C.Cu2+ D.Ag+
(2)三种盐的化学式分别是A ,B ,C .
(3)不需要加入任何试剂就能将上述三种盐溶液区分开来,鉴别出来的先后顺序为 (填化学式).
(4)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1:2:3:4,则A、B、C三种盐的物质的量之比为 ,若向溶液中加入过量Ba(OH)2,发生反应的总离子方程式为 .
| 阳离子 | NH4+、Mg2+、Ba2+ |
| 阴离子 | OH-、NO3-、Cl- |
(2)甲是
Ⅱ.有A、B、C三种可溶性盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C的顺序依次增大.将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀.请回答下列问题:
(1)经检验,三种盐中还含有下列选项中的一种离子,该离子是
A.Na+ B.Mg2+ C.Cu2+ D.Ag+
(2)三种盐的化学式分别是A
(3)不需要加入任何试剂就能将上述三种盐溶液区分开来,鉴别出来的先后顺序为
(4)若将A、B、C三种盐按一定比例溶于水,所得溶液中只含有Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1:2:3:4,则A、B、C三种盐的物质的量之比为
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:Ⅰ.(1)由于甲、乙、丙是三种不含相同离子的可溶性强电解质,故NH4+、Mg2+对应的阴离子均不能是OH-,故OH-对应的阳离子是Ba2+,即化合物为Ba(OH)2;另外两种化合物可能为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,取等质量的三种化合物配制相同体积的溶液,根据溶质物质的量浓度:c(甲)>c(乙)>c(丙),得出摩尔质量的大小关系,据此分析出丙;
(2)甲和乙为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,根据甲的摩尔质量最小,得出甲可能为:NH4NO3或NH4Cl;根据NH4NO3和NH4Cl的阴离子的不同,来分析确定方法;
(3)等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀,A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大,则A为盐酸盐,B为硝酸银,C为硫酸盐;等物质的量混合,生成沉淀可能为AgCl,则A为FeCl3,B为AgNO3,C为K2SO4,以此来解答.
(2)甲和乙为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,根据甲的摩尔质量最小,得出甲可能为:NH4NO3或NH4Cl;根据NH4NO3和NH4Cl的阴离子的不同,来分析确定方法;
(3)等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀,A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大,则A为盐酸盐,B为硝酸银,C为硫酸盐;等物质的量混合,生成沉淀可能为AgCl,则A为FeCl3,B为AgNO3,C为K2SO4,以此来解答.
解答:
解:Ⅰ.(1)由于甲、乙、丙是三种不含相同离子的可溶性强电解质,故NH4+、Mg2+对应的阴离子均不能是OH-,故OH-对应的阳离子是Ba2+,即化合物为Ba(OH)2;另外两种化合物可能为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),故摩尔质量M(甲)<M(乙)<M(丙),而摩尔质量最大的是Ba(OH)2,故丙为Ba(OH)2,故答案为:Ba(OH)2;
(2)甲和乙为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,而甲的摩尔质量最小,故甲可能为:NH4NO3或NH4Cl;而NH4NO3和NH4Cl的阴离子不同,故甲的确定的方法:取少量甲溶液于试管中,向其中滴加适量的硝酸银溶液,若有白色沉淀生成,则证明为NH4Cl,反之则为NH4NO3,
故答案为:NH4NO3或NH4Cl,取少量甲溶液于试管中,向其中滴加适量的硝酸银溶液,若有白色沉淀生成,则证明为NH4Cl,反之则为NH4NO3;
Ⅱ.等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀,A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大,则A为盐酸盐,B为硝酸银,C为硫酸盐;等物质的量混合,生成沉淀可能为AgCl,则A为FeCl3,B为AgNO3,C为K2SO4,
(1)由上述分析可知,正盐中含Ag+,三种阴离子与A、B、C中的阳离子均不会生成沉淀,故答案为:D;
(2)由上述分析可知,A为FeCl3,B为AgNO3,C为K2SO4,故答案为:FeCl3;AgNO3;K2SO4;
(3)观察黄色的溶液为FeCl3,与FeCl3反应生成白色沉淀的为AgNO3,最后可知K2SO4,则检验顺序为FeCl3、AgNO3、K2SO4,故答案为:FeCl3、AgNO3、K2SO4;
(4)Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1:2:3:4,设FeCl3为1mol,则AgNO3为3mol,K2SO4为2mol,A、B、C三种正盐的物质的量之比为1:3:2,向溶液中加入过量Ba(OH)2,Ba2+和OH-是过量的,故应根据Fe3+和SO42-的量来确定消耗的Ba2+和OH-量,故离子方程式为:Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓,故答案为:1:3:2,Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓.
(2)甲和乙为NH4NO3、MgCl2或NH4Cl、Mg(NO3)2,而甲的摩尔质量最小,故甲可能为:NH4NO3或NH4Cl;而NH4NO3和NH4Cl的阴离子不同,故甲的确定的方法:取少量甲溶液于试管中,向其中滴加适量的硝酸银溶液,若有白色沉淀生成,则证明为NH4Cl,反之则为NH4NO3,
故答案为:NH4NO3或NH4Cl,取少量甲溶液于试管中,向其中滴加适量的硝酸银溶液,若有白色沉淀生成,则证明为NH4Cl,反之则为NH4NO3;
Ⅱ.等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀,A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大,则A为盐酸盐,B为硝酸银,C为硫酸盐;等物质的量混合,生成沉淀可能为AgCl,则A为FeCl3,B为AgNO3,C为K2SO4,
(1)由上述分析可知,正盐中含Ag+,三种阴离子与A、B、C中的阳离子均不会生成沉淀,故答案为:D;
(2)由上述分析可知,A为FeCl3,B为AgNO3,C为K2SO4,故答案为:FeCl3;AgNO3;K2SO4;
(3)观察黄色的溶液为FeCl3,与FeCl3反应生成白色沉淀的为AgNO3,最后可知K2SO4,则检验顺序为FeCl3、AgNO3、K2SO4,故答案为:FeCl3、AgNO3、K2SO4;
(4)Fe3+、SO42-、NO3-、K+四种离子且物质的量之比依次为1:2:3:4,设FeCl3为1mol,则AgNO3为3mol,K2SO4为2mol,A、B、C三种正盐的物质的量之比为1:3:2,向溶液中加入过量Ba(OH)2,Ba2+和OH-是过量的,故应根据Fe3+和SO42-的量来确定消耗的Ba2+和OH-量,故离子方程式为:Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓,故答案为:1:3:2,Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓.
点评:本题考查物质检验和鉴别的实验方案的设计,为高频考点,注意三种阴离子的摩尔质量推断物质为解答的关键,侧重分析能力及推断能力的考查,题目难度中等.

练习册系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
| B、醋酸溶液除水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、过氧化钠与水反应:2O22-+2H2O═4OH-+O2↑ |
| D、向NaAlO2溶液中滴加NaHCO3溶液HCO3-+AlO2-+H2O=A(OH)3↓+CO32- |
2012年2月6日,在辽宁沈阳至本溪段的丹霞公路发生了应雾大路滑而引起汽车追尾的重大的交通事故.雾属于下列哪种分散系( )
| A、乳浊液 | B、溶液 |
| C、胶体 | D、悬浊液 |
某气体由常见的一种或多种气体组成,经测定其中只含有碳、氧两种元素,碳、氧元素的质量比为3:8,则关于该气体的说法正确的是( )
| A、该气体一定是纯净物 |
| B、该气体一定是CO、CO2的混合物 |
| C、该气体中所含的物质最多只有2种 |
| D、该气体的组成情况可能有3种组合 |
分子式为C6H10的有机物其结构不可能是( )
| A、含有一个双键的直链有机物 |
| B、含有两个双键的直链有机物 |
| C、含有一个双键的环状有机物 |
| D、含有两个环的环状有机物 |
氯气溶于水达到平衡后,下列叙述中正确的是( )
| A、通入少量SO2,溶液的漂白性增强 | ||
| B、加入少量Na2CO3粉末或CaCO3粉末,c(H+)减小,HClO浓度增大 | ||
| C、加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-) | ||
D、再加入少量水,
|
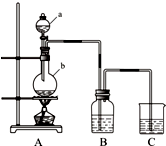 利用如图所示装置制备饱和氯水,探究新制饱和氯水的组成和性质而进行了科学实验:先对制得的氯水进行观察,再用胶头滴管将该氯水逐滴滴入盛有含酚酞的NaOH溶液的试管中,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液.据此回答:
利用如图所示装置制备饱和氯水,探究新制饱和氯水的组成和性质而进行了科学实验:先对制得的氯水进行观察,再用胶头滴管将该氯水逐滴滴入盛有含酚酞的NaOH溶液的试管中,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液.据此回答: