题目内容
根据原子结构的有关知识和元素周期律,思考并回答有关114号元素的几个问题
(1)原子核外有几个电子层?最外层电子数可能是多少?
(2)它在周期表中位于第几周期、第几族?
(3)它属于金属元素还是非金属元素?
(1)原子核外有几个电子层?最外层电子数可能是多少?
(2)它在周期表中位于第几周期、第几族?
(3)它属于金属元素还是非金属元素?
考点:元素周期表的结构及其应用
专题:
分析:根据电子排布规律写出该原子原子结构示意图,根据电子层数判断周期数,根据价电子判断所属族数,根据在周期表中的位置判断是否是金属.
解答:
解:该原子的原子结构示意图为: ,电子层数=周期数,最外层电子数=族序数,在铅元素下方,金属性比铅强,属金属,
,电子层数=周期数,最外层电子数=族序数,在铅元素下方,金属性比铅强,属金属,
答:(1)原子核外有七个电子层.最外层电子数是4;
(2)它在周期表中位于第七周期、第IVA族;
(3)它属于金属元素.
 ,电子层数=周期数,最外层电子数=族序数,在铅元素下方,金属性比铅强,属金属,
,电子层数=周期数,最外层电子数=族序数,在铅元素下方,金属性比铅强,属金属,答:(1)原子核外有七个电子层.最外层电子数是4;
(2)它在周期表中位于第七周期、第IVA族;
(3)它属于金属元素.
点评:本题考查根据原子结构示意图,判断判断元素所属周期和族,比较容易.

练习册系列答案
相关题目
下列各组离子,在溶液中一定能大量共存的是( )
| A、K+、H+、Cl-、OH- |
| B、Ba2+、Na+、SO42-、NO3- |
| C、Na+、Ca2+、NO3-、CO32- |
| D、Na+、Cu2+、Cl-、NO3- |
下列说法中,正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、放热反应在常温下一定能很容易发生 |
| C、吸热反应在一定条件下也能自发进行 |
| D、氧化还原反应一定是放热反应 |
用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个.下列关于R的描述中正确的是( )
| A、R的氧化物一定能溶于水 |
| B、R的最高价氧化物所对应的水化物一定是H2RO3 |
| C、R的氧化物一定能与NaOH溶液反应 |
| D、R是非金属元素 |
已知R2+核外有a个电子,b个中子.表示R原子符号正确的是( )
| A、bR |
| B、a-2R |
| C、a+2R |
| D、a-2R |
下列各组中化合物的性质比较,不正确的是( )
| A、酸性:HClO4>HBrO4>HIO4 |
| B、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C、稳定性:PH3<H2S<HCl |
| D、熔沸点:H2O<H2S<H2Se<H2Te |
下列离子方程式中,正确的是( )
| A、稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| B、氧化铜与稀盐酸反应:CuO+2H+=Cu2++H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、稀盐酸与碳酸钠溶液反应:Na2CO3+2H+=2Na++H2O+CO2↑ |
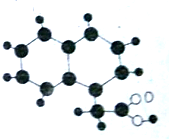 2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图.不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键.下列有关M的推断正确的是( )
2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图.不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键.下列有关M的推断正确的是( )| A、M的分子式为C12H12O2 |
| B、M与足量氢气在一定条件下反应的产物的环上一氯代物有7种 |
| C、M能发生中和反应、取代反应 |
| D、一个M分子最多有11个原子共面 |