题目内容
常温下,有关下列4种溶液的说法正确的是
| ① | ② | ③ | ④ |
| 0.1 mol·L-1氨水 | pH=11氨水 | 0.1 mol·L-1盐酸 | pH=3盐酸 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍,pH与②相同
C.①与③混合,若溶液pH=7,则溶液中c(NH4+)>c(Cl-)
D.②与④等体积混合,混合液pH>7
D
解析试题分析:A、盐酸是强酸,氨水是弱碱,因此在浓度相同的条件下,盐酸对水的电离抑制程度大,即由水电离出的c(H+):③<①,A不正确;B、氨水是弱碱,0.1 mol·L-1氨水稀释到原来的100倍浓度是0.001mol/L,其溶液的pH值小于11,B不正确;C、①与③混合,若溶液pH=7,则根据电荷守恒可知溶液中c(NH4+)=c(Cl-),C不正确;D、②与④等体积混合后氨水过量溶液显碱性,因此混合液pH>7,D正确,答案选D。
考点:考查弱电解质的电离、溶液中离子浓度大小比较以及pH计算

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
一定温度下,卤化银AgX(X:Cl—、Br—、I—)及Ag2CrO4的沉淀溶解平衡曲线如图所示。横坐标p(Ag+)表示“-lgc(Ag+)”,纵坐标Y表示“ -lgc(X-)”或“-lgc(CrO42—)”。下列说法正确的是
| A.a点表示c(Ag+)=c(CrO42—) |
| B.b点可表示AgI的饱和溶液 |
| C.该温度下AgI的Ksp约为1×10—16 |
| D.该温度下AgCl、AgBr饱和溶液中:c(Cl—)<c(Br—) |
下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
| A.两条曲线间任意点均有c(H+)×c(OH-)=KW |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |
对于0.1 mol·L-1 Na2SO3溶液,正确的是( )
| A.升高温度,溶液的pH降低 |
| B.c(Na+)=2c(SO32―)+c(HSO3-)+c(H2SO3) |
| C.c(Na+)+c(H+)=2c(SO32―)+2c(HSO3-)+c(OH―) |
| D.加入少量NaOH固体,c(SO32―)与c(Na+)均增大 |
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
B.溶液中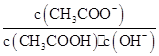 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH=7 |
已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A.该溶液的pH=4 |
| B.升高温度,溶液的pH增大 |
| C.此酸的电离平衡常数约为1×10-7 |
| D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列关于电解质溶液的叙述正确的是 ( )。
| A.常温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液的pH大 |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C.中和pH与体积均相同的盐酸和醋酸,消耗NaOH溶液的物质的量相同 |
| D.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
下列有关说法正确的是( )
| A.常温下,0.1 mol/L NH4Cl溶液加蒸馏水稀释,溶液的pH不断增大,但无限接近7 |
| B.25 ℃时,溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14 |
| C.pH=6的纯水中,c(OH-)=10-8 mol·L-1 |
| D.稀释0.01 mol·L-1的醋酸溶液时,溶液中所有的离子浓度均减小 |