��Ŀ����
������ʾ����һ�������»ǰ�������Ph=0.5��2.5��Χ�ھ����ȶ����ڣ���ҵ�����������ȡ����ͭ������ʾ��ͼ���£�
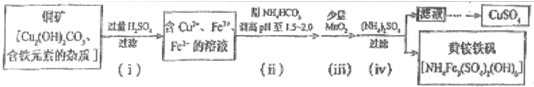
�������������������
��1�����裨���������Լ������pH���õ������� �������ӷ��ţ�
��2���ڲ��裨���������ķ�Ӧ�У�����������MnO2�������� ��
��3�����裨������ȥ���ʵ����ӷ���ʽ�ɱ�ʾΪ ��
��4��ʵ����ģ����ʽ̼��ͭ��Cu2��OH��2CO3�����Ʊ�������Թ��м���̼������Һ������ͭ��Һ��ˮԡ������70�����ң���0.4mol/L��NaOH��Һ����pH��8.5�������á����ˡ�����ˮϴ�ӡ���ɣ��õ���ʽ̼��ͭ��Ʒ������������ʽ̼��ͭ���Ʊ�������������������⣺
�ٹ��˺�ϴ�ӵ�Ŀ����ʲô ���������ϴ�ӳ��� ��
����ʵ��õ�a g��Ʒ��ֻ��CuO���ʣ�ȡ����Ʒ�������ֽ���ȫ�õ�bg���壬����Ʒ�м�ʽ̼��ͭ�ķ����� ��

�������������������
��1�����裨���������Լ������pH���õ�������
��2���ڲ��裨���������ķ�Ӧ�У�����������MnO2��������
��3�����裨������ȥ���ʵ����ӷ���ʽ�ɱ�ʾΪ
��4��ʵ����ģ����ʽ̼��ͭ��Cu2��OH��2CO3�����Ʊ�������Թ��м���̼������Һ������ͭ��Һ��ˮԡ������70�����ң���0.4mol/L��NaOH��Һ����pH��8.5�������á����ˡ�����ˮϴ�ӡ���ɣ��õ���ʽ̼��ͭ��Ʒ������������ʽ̼��ͭ���Ʊ�������������������⣺
�ٹ��˺�ϴ�ӵ�Ŀ����ʲô
����ʵ��õ�a g��Ʒ��ֻ��CuO���ʣ�ȡ����Ʒ�������ֽ���ȫ�õ�bg���壬����Ʒ�м�ʽ̼��ͭ�ķ�����
���㣺���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ��,ͭ����������Ҫ���������Ҫ����
ר�⣺ʵ�������
��������1��������識�����Һ�е�����ҺPH��Ϊ�˺�i�����м���Ĺ������ᷴӦͬʱ�����ҺPH���ڳ�ȥ�����ӣ�笠����Ӳ���Ӧ��������̼��������ӣ�
��2��Fe2+���л�ԭ�ԣ����Ա�MnO2������������������Fe3+��
��3����������麟�ȥFe3+���ʣ�
��4����ϴ�ӿɳ�ȥ��ʽ̼��ͭ����������������ƣ�����Ϊ���Ų�������©���м�����ˮ���պý�û������������ˮ�������ظ�2-3�μ��ɣ�
�����ʽ̼��ͭ����������Ϊx�����ݷ�ӦCu2��OH��2CO3
2CuO+H2O+CO2�������ó������������ʽ�������ʽ̼��ͭ������������
��2��Fe2+���л�ԭ�ԣ����Ա�MnO2������������������Fe3+��
��3����������麟�ȥFe3+���ʣ�
��4����ϴ�ӿɳ�ȥ��ʽ̼��ͭ����������������ƣ�����Ϊ���Ų�������©���м�����ˮ���պý�û������������ˮ�������ظ�2-3�μ��ɣ�
�����ʽ̼��ͭ����������Ϊx�����ݷ�ӦCu2��OH��2CO3
| ||
���
�⣺ͭ����Ҫ�ɷ�Ϊ��ʽ̼��ͭ����������Ԫ�ص����ʣ�������������ᣬCu2��OH��2CO3+2H2SO4=2CuSO4+3H2O+CO2�������ˣ���Һ����Ҫ��������ͭ��������������������������̼����泥������MnSO4��ת���ʣ�ʹMnCO3������ȫ������PH1.5-2.0�������Թ�����NH4HCO3��Һ��pH�����ͣ�H+����MnCO3��NH4HCO3��Ӧ������������ǿ�������������̣����Ժ��������ӷ���������ԭ��Ӧ���������ӱ�����Ϊ�����ӣ���������麟�ȥ���ʷ�ӦΪ��3Fe3++NH4++2SO42-+6H2O=NH4Fe3��SO4��2��OH��6��+6H+�������ˣ���ҺΪ����ͭ��ͨ���ᾧ��ȡ����ͭ��
��1����ĿҪ�����PH��笠����������ԣ�̼����������Լ��ԣ��������õ�������̼��������ӣ�
�ʴ�Ϊ��HCO3-��
��2��Fe2+���л�ԭ�ԣ����Ա�MnO2������������������Fe3+��2mol Fe2+ת�Ƶ���2 mol������Fe3+��1mol MnO2ת�Ƶ���2 mol����Ӧ�����ӷ���ʽΪ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O���Ա��ڲ��裨�������γɳ�����
�ʴ�Ϊ������Һ�е�Fe2+ת��ΪFe3+��
��3����������泥�����狀������������γɳ�������ӦΪ��3Fe3++NH4++2SO42-+6H2O=NH4Fe3��SO4��2��OH��6��+6H+��
�ʴ�Ϊ��3Fe3++NH4++2SO42-+6H2O=NH4Fe3��SO4��2��OH��6��+6H+��
��4���ٳ�������������Һ�е�Na+��SO42-������������ϴ�ӣ����˺���©�������м�����������ˮ��ʹҺ��պ�û������������ϴ���������IJ�Һ�����ã���Һ�����£��ظ�����2-3�Σ���֤ϴ�Ӹɾ���
�ʴ�Ϊ����ȥ��������������Na+��SO42-�����Ų�������©���м�����ˮ���պý�û������������ˮ�������ظ�2-3�μ��ɣ�
�ڼ�ʽ̼��ͭ��ȫ�ֽ�õ�CuO������Ʒ�м�ʽ̼��ͭ����������Ϊx��
���ݼ�ʽ̼��ͭ�ķ���ʽ��Cu2��OH��2CO3
2CuO+H2O+CO2�� �������m
222 18 44 ��18+44��=62
ax ��a-b��
�ɵ�
=
�����x=
�������Ʒ�м�ʽ̼��ͭ�ķ�����
��100%��
�ʴ�Ϊ��
��100%��
��1����ĿҪ�����PH��笠����������ԣ�̼����������Լ��ԣ��������õ�������̼��������ӣ�
�ʴ�Ϊ��HCO3-��
��2��Fe2+���л�ԭ�ԣ����Ա�MnO2������������������Fe3+��2mol Fe2+ת�Ƶ���2 mol������Fe3+��1mol MnO2ת�Ƶ���2 mol����Ӧ�����ӷ���ʽΪ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O���Ա��ڲ��裨�������γɳ�����
�ʴ�Ϊ������Һ�е�Fe2+ת��ΪFe3+��
��3����������泥�����狀������������γɳ�������ӦΪ��3Fe3++NH4++2SO42-+6H2O=NH4Fe3��SO4��2��OH��6��+6H+��
�ʴ�Ϊ��3Fe3++NH4++2SO42-+6H2O=NH4Fe3��SO4��2��OH��6��+6H+��
��4���ٳ�������������Һ�е�Na+��SO42-������������ϴ�ӣ����˺���©�������м�����������ˮ��ʹҺ��պ�û������������ϴ���������IJ�Һ�����ã���Һ�����£��ظ�����2-3�Σ���֤ϴ�Ӹɾ���
�ʴ�Ϊ����ȥ��������������Na+��SO42-�����Ų�������©���м�����ˮ���պý�û������������ˮ�������ظ�2-3�μ��ɣ�
�ڼ�ʽ̼��ͭ��ȫ�ֽ�õ�CuO������Ʒ�м�ʽ̼��ͭ����������Ϊx��
���ݼ�ʽ̼��ͭ�ķ���ʽ��Cu2��OH��2CO3
| ||
222 18 44 ��18+44��=62
ax ��a-b��
�ɵ�
| 222 |
| 62 |
| ax |
| a-b |
| 111(a-b) |
| 31a |
| 111(a-b) |
| 31a |
�ʴ�Ϊ��
| 111(a-b) |
| 31a |
���������⿼���˹������̵ķ����жϣ���Ҫ���������ʵķ��롢�ᴿ��ʵ����ƣ�������ѧ���ķ���������ʵ�������Ŀ��飬Ϊ�߿��������ͣ�ע����������Ϣ��������ʵ����ʵ���ͬ�����⣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
���и���Ԫ���γɵĵ�����������ǿ���ǣ�������
| A��ԭ�Ӻ���δ�ɶԵ������ĵڶ�����Ԫ�� |
| B��λ�����ڱ��е������ڢ�A���Ԫ�� |
| C��ԭ�����������Ų�Ϊ3s23p3��Ԫ�� |
| D��ԭ�����������Ų�Ϊ2s22p4��Ԫ�� |

 ���ԭ���ڹ�ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڹ�ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺