题目内容
某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物;②煤和石油都是可再生能源;
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;④不锈钢和目前流通的硬币都是合金:
⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;⑥豆浆和雾都是胶体。
上述说法正确的是
A.①②④⑤ B.①②⑤⑥ C.①③④⑥ D.②③④⑤
C
【解析】
试题分析:①漂白粉是氯化钙和次氯酸钙的混合物,酸雨是二氧化硫的水溶液都是混合物,故①正确;②可再生能源是指在自然界中可以不断再生、永续利用的能源,煤和石油都不是可再生能源,故②错误;③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质,③正确;④不锈钢和目前流通的硬币都是合金,故④正确;⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、盐、盐和氧化物,故⑤错误;⑥豆浆和雾都是胶体,故⑥正确;综上所述:①③④⑥正确;故选C。
考点:考查纯净物混合物的概念区别,能源的分类,合金的组成,胶体的本质特征等

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(8分)硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
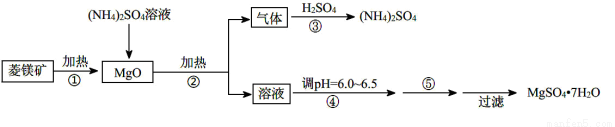
(1)步骤②中发生反应的离子方程式为 。
(2)步骤④中调节pH=6.0~6.5的目的是 。
(3)步骤⑤的操作为
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为 [25℃时,Ksp[Mg(OH)2] =5.6×10-12]。


 >H2CO3>
>H2CO3>
 综合考虑反应物的转化率和原料成本等因素,将
综合考虑反应物的转化率和原料成本等因素,将 转变为
转变为 的最佳方法是
的最佳方法是


 ②
② ③
③ ④
④ ⑤
⑤