题目内容
(本题共10分)(一)(6分)中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出)。单质A常作为食品包装材料,甲是两性氧化物。

根据图示转化关系回答:
(1)写出下列物质的化学式:单质A_______________,乙_______________。
(2)写出单质A与Fe2O3反应的化学方程式: ,利用该反应的原理,可用于______________________________。
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是____________________________。
(4)写出反应①的离子方程式:_____________________________________________。
(二)(4分)(5)工业上冶炼下列物质通常不采用电解法的是 。
a.Na b.Mg c.Fe d.Ag
(6)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有( )
a.KCl b. KClO 3 c. MnO2 d. Mg
(1)Al NaAlO2 (2)2Al + Fe2O3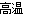 Al2O3 + 2Fe 焊接钢轨等
Al2O3 + 2Fe 焊接钢轨等
(3)Al单质遇浓硫酸发生钝化 (4)2Al + 2OH-+ 2H2O=2AlO2-+ 3H2↑ (5)cd (6) bd
【解析】
试题分析:(一)单质A常作为食品包装材料,因此A是铝;甲是两性氧化物,则甲为氧化铝。铝鱼 氢氧化钠反应生成偏铝酸钠和氢气,所以B是氢气,乙是偏铝酸钠,氧化铝与氢氧化钠反应生成偏铝酸钠和水,则丙是水。
(1)A和乙的化学式分别为Al、NaAlO2。
(2)单质铝与Fe2O3发生铝热反应的化学方程式为2Al + Fe2O3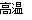 Al2O3 + 2Fe,利用该反应的原理,可用于焊接钢轨、冶炼难溶金属等等。
Al2O3 + 2Fe,利用该反应的原理,可用于焊接钢轨、冶炼难溶金属等等。
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是常温下Al单质遇浓硫酸发生钝化。
(4)反应①的离子方程式为(4)2Al + 2OH-+ 2H2O=2AlO2-+ 3H2↑。
(二)(5)钠和镁是活泼的金属需要电解法冶炼,铁可以用还原剂还原,银是不活泼的金属,一般用热分解,答案选cd。
(6)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有镁条和氯酸钾,答案选bd。
考点:考查无机框图题推断以及铝热反应、金属冶炼等等

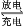 Fe(OH)2+Ni(OH)2,
Fe(OH)2+Ni(OH)2, Ni(OH)2
Ni(OH)2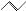 ,有机物X的键线式为
,有机物X的键线式为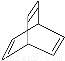 ,下列说法不正确的是
,下列说法不正确的是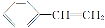
 B.
B. C.CH4O D.C
C.CH4O D.C