题目内容
17.下列物质A~N均为中学化学中常见物质,其A、B、C是三种常见金属,F、G、J、E均为氧化物,F是淡黄色固体,其焰色反应为黄色,E在常温下是无色液体,D、I都是无色气体,L为白色胶状沉淀.在适当的条件下,它们之间可以发生如下图所示的转化(部分产物被略去).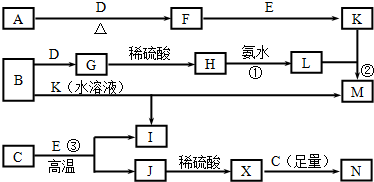
试回答下列问题:
(1)列举F的一种重要用途:用于呼吸面具或潜水艇中作为氧气的来源
(2)反应③的化学方程式是:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2
(3)反应①的离子方程式是:Al3++3NH3•H2O=Al(OH)3↓+3NH4+
(4)反应②的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O
(5)为检验N中含有的Fe2+,取少量N的溶液,向其中加入KSCN溶液,振荡后,再加入氯水(或H2O2)后,溶液立即呈血红色.
分析 F是淡黄色固体,且且是因氧化物,其焰色反应为黄色,则F为Na2O2,金属A与气体D反应生成F,则A为Na、D为O2,氧化物E在常温下是无色液体,与过氧化钠反应生成K,则B是H2O、K是NaOH.金属B与氧气反应生成氧化物G,G能与硫酸反应生成H,H与氨水反应得到白色胶状沉淀L,则B为Al、G为Al2O3、H为Al2(SO4)3、L为Al(OH)3、M为NaAlO2、无色气体I为H2.金属C与E在高温下生成氢气与J,J与硫酸反应生成X为硫酸盐,而X能与C反应得到N,说明金属C为变价金属,则C为Fe,Fe3O4,X为FeSO4和Fe2(SO4)3的混合溶液,N为FeSO4,据此解答.
解答 解:F是淡黄色固体,且且是因氧化物,其焰色反应为黄色,则F为Na2O2,金属A与气体D反应生成F,则A为Na、D为O2,氧化物E在常温下是无色液体,与过氧化钠反应生成K,则B是H2O、K是NaOH.金属B与氧气反应生成氧化物G,G能与硫酸反应生成H,H与氨水反应得到白色胶状沉淀L,则B为Al、G为Al2O3、H为Al2(SO4)3、L为Al(OH)3、M为NaAlO2、无色气体I为H2.金属C与E在高温下生成氢气与J,J与硫酸反应生成X为硫酸盐,而X能与C反应得到N,说明金属C为变价金属,则C为Fe,Fe3O4,X为FeSO4和Fe2(SO4)3的混合溶液,N为FeSO4.
(1)F为Na2O2,F的一种重要用途:用于呼吸面具或潜水艇中作为氧气的来源,
故答案为:用于呼吸面具或潜水艇中作为氧气的来源;
(2)反应③的化学方程式是:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(3)反应①的离子方程式是:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(4)反应②的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(5)为检验N中含有的Fe2+,取少量N的溶液,向其中加入KSCN溶液,振荡后,再加入 氯水(或H2O2)后,溶液立即呈血红色,
故答案为:氯水(或H2O2)后;血红色.
点评 本题考查无机物的推断,题目难度中等,注意根据物质的颜色、反应的现象、特殊反应等为突破口进行推断,学习中注意元素化合物的性质,注重相关知识的积累.

(1)电解饱和食盐水是生产H2的方法之一.常温下,电解200mL饱和食盐水一段时间后,溶液质量减轻0.73g(假设气体全部逸出).生产氢气在标准状况下的体积为224mL.
(2)在电弧炉中,甲烷裂解产生乙炔和氢气,若1m3甲烷此过程生成0.24m3氢气,则甲烷的裂解率为16%(体积均在相同条件下测定).
(3)已知:CxH7+H2O→CO+CO2+H2(未配平).工业上用甲烷、乙烷的混合气体利用上述反应生产氢气,反应后气体经干燥组成如表所示.
| 组分 | CO | CO2 | H2 |
| 体积分数 | 20% | 5% | 75% |
(4)合成氨生产过程中,消耗氮氢混合气2800m3(其中CH4的体积分数为0.2%,下同),分离液氨后的氮氢混合气中含CH43%.计算分离出液氨为多少吨(保留2位小数,所有体积均已折算至标准状况).
方案一:用下列流程测定铁触媒的含铁量,确定其组成.

(1)步骤④后面需用酸式滴定管(填仪器名称)取25.00mL稀释后溶液.
(2)因为通入Cl2不足量,“溶液B”中还含有FeCl2 或者FeSO4或者Fe2+会影响测定结果.
(3)因为通入Cl2过量且加热煮沸不充分,“溶液B”中可能含有Cl2.请设计实验方案检验Cl2,完成下列实验报告.限选试剂:0.1mol•L-1酸性KMnO4溶液、紫色石蕊试液、品红稀溶液、淀粉-KI溶液、0.1moL•L-1KSCN溶液.
| 实验操作 | 实验现象与结论 |

(4)“干燥管C”的作用是防止空气中的CO2和水蒸气进入B中.
(5)称取15.2g铁触媒进行上述实验.充分反应后,测得“干燥管B”增重11.0g,则该铁触媒的化学式可表示为Fe4O5或2FeO•Fe2O3.(相对原子质量:C-12 O-16 Fe-56)
| A. | 食盐水 | B. | 碘酒 | C. | 淀粉溶液 | D. | Fe(OH)3沉淀 |
| A. | CO2 | B. | MgCl2 | C. | BF3 | D. | PCl3 |
(1)A、B、C的电负性由小到大的顺序为C<O<N(用元素符号表示).
(2)D元素的原子核外共有12种不同运动状态的电子、4种不同能级的电子.
(3)写出E的基态原子的电子排布式:1s22s22p63s23p64s2.
(4)F和X(质子数为25)两元素的部分电离能数据列于下表:比较两元素的I2、I3可知,气态X2+再失去一个电子比气态F2+再失去一个电子难.对此,你的解释是Mn2+的3d轨道电子排布为半满状态较稳定,而Fe2+的3d轨道电子数为6,不是较稳定状态.
| 元素 | X | F | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| A. | 元素的相对原子质量逐渐增大 | B. | 核外电子排布呈现周期性变化 | ||
| C. | 原子半径呈现周期性变化 | D. | 元素化合价呈现周期性变化 |
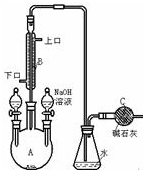 制备溴苯的实验装置如图所示,回答下列问题:
制备溴苯的实验装置如图所示,回答下列问题: