题目内容
7.元素的性质呈现周期性变化的根本原因是( )| A. | 元素的相对原子质量逐渐增大 | B. | 核外电子排布呈现周期性变化 | ||
| C. | 原子半径呈现周期性变化 | D. | 元素化合价呈现周期性变化 |
分析 根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答 解:A.因随原子的相对原子质量的递增,元素发生变化,但不能说明周期性变化,故A错误;
B.原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故B正确;
C.原子半径是元素的性质,不能解释元素性质的周期性变化,故C错误;
D.元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故D错误;
故选:B.
点评 本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,注意不能用元素本身的性质来解释元素性质的周期性变化.

练习册系列答案
相关题目
18.用化学方法除去下列物质中的杂质(括号内为杂质),填写所加试剂和有关离子反应方程式.
| 试剂 | 离子反应方程式 | |
| ①Mg(Al) | ||
| ②FeCl2溶液(FeCl3) | ||
| ③NaHCO3(Na2CO3) |
15.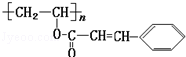 某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
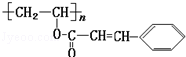 某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】
某种“光敏性高分子”材料在荧光屏及大规模集成电路中应用广泛.其结构可表示为:对该“光敏性高分子”叙述正确的是( )【-COO-基团与氢气不反应】| A. | 化学式为(C11H11O2)n | |
| B. | 它能发生还原反应 | |
| C. | 它可以和FeCl3溶液发生显色反应 | |
| D. | 1mol该分子最多能和4molH2发生加成反应 |
12.优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2一乙烯吡啶(简写P2VP)和I2 的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为2Li+P2VP•nI2═P2VP•(n-1)I2+2LiI,则下列说法正确的是( )
| A. | 聚2一乙烯吡啶的复合物与有机物性质相似,因此聚2一乙烯吡啶的复合物不会导电 | |
| B. | 正极的反应为P2VP•nI2+2Li++2e-═P2VP•(n-1)I2+2LiI | |
| C. | 电池工作时,碘离子移向P2VP一极 | |
| D. | 该电池所产生的电压低,使用寿命比较短 |
19.下列微粒中,电子层结构完全相同的一组是( )
| A. | S2-、Cl-、K+ | B. | Cl-、Br-、I- | C. | Na+、Mg2+、Cl- | D. | O2-、Mg2+、Cl- |
16.2007年诺贝尔化学奖授予善于做“表面文章”的德国科学家格哈德•埃特尔.他的成就之一是证实了气体在固体催化剂表面进行的反应,开创了表面化学的方法论.在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示.下列说法正确的是( )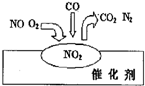

| A. | NO2是该过程的最终产物 | |
| B. | NO和O2必须在催化剂表面才能反应 | |
| C. | 汽车尾气的主要污染成分是CO2和NO | |
| D. | 该催化转化的总反应方程式为:2NO+O2+4CO$\frac{\underline{\;催化剂\;}}{\;}$ 4CO2+N2 |
17.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色.五种元素核电荷数之和为54,最外层电子数之和为20.W、Z最外层电子数相同,Z的核电荷数是W的2倍.工业上一般通过电解氧化物的方法获得Y的单质.则下列说法不正确的是( )
| A. | 原子半径:X>Y>Q>W | |
| B. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| C. | X 与W能形成两种常见的化合物 | |
| D. | Y单质既能与盐酸反应,又能与氢氧化钠溶液反应 |