题目内容
已知琥珀酸亚铁是常见的治疗缺铁性贫血的补铁药剂的主要成分,该药品不溶于水但能溶于人体中的胃酸(已知三价铁离子不具有治疗贫血的功能),请回答相关问题:
(1)常见治疗缺铁性贫血的补铁药剂通常都制成糖衣片,除了服用方便外它的另一个最重要的原因是 .
(2)某同学为了检测某补铁药剂药片中Fe2+的存在,设计并进行了如下实验:
a、将药片去除糖衣,碾碎.
b、将碾碎的药片粉末转移到锥形瓶中,加入试剂A,过滤,得浅绿色溶液
c、向滤液中加入硫氰化钾溶液,溶液呈淡红色,加入几滴新制氯水,溶液立即出现血红色
d、向血红色溶液中继续滴加氯水,并振荡,静止几分钟,红色褪去.请回答下列问题:
①操作a中碾碎药片所使用的主要仪器是 ;
②试剂A是 ,
③加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 .
④用方程式表示溶液出现血红色的原因 .
⑤对溶液最后褪色的原因,甲、乙两位同学首先进行了猜想:
甲同学认为:可能是溶液中的+3价Fe又被还原为+2价Fe
乙同学认为:可能是溶液中的SCN-被过量的氯水氧化
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确.写出有关的实验操作、预期现象和结论. .
(1)常见治疗缺铁性贫血的补铁药剂通常都制成糖衣片,除了服用方便外它的另一个最重要的原因是
(2)某同学为了检测某补铁药剂药片中Fe2+的存在,设计并进行了如下实验:
a、将药片去除糖衣,碾碎.
b、将碾碎的药片粉末转移到锥形瓶中,加入试剂A,过滤,得浅绿色溶液
c、向滤液中加入硫氰化钾溶液,溶液呈淡红色,加入几滴新制氯水,溶液立即出现血红色
d、向血红色溶液中继续滴加氯水,并振荡,静止几分钟,红色褪去.请回答下列问题:
①操作a中碾碎药片所使用的主要仪器是
②试剂A是
③加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是
④用方程式表示溶液出现血红色的原因
⑤对溶液最后褪色的原因,甲、乙两位同学首先进行了猜想:
甲同学认为:可能是溶液中的+3价Fe又被还原为+2价Fe
乙同学认为:可能是溶液中的SCN-被过量的氯水氧化
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确.写出有关的实验操作、预期现象和结论.
考点:性质实验方案的设计,二价Fe离子和三价Fe离子的检验
专题:几种重要的金属及其化合物
分析:(1)亚铁盐不稳定,易被空气中氧气氧化生成铁盐;
(2)①用于研碎药片的仪器是研钵;
②琥珀酸亚铁不溶于水,要检验亚铁离子应该加入酸将琥珀酸亚铁转化为可溶性的亚铁盐;
③亚铁离子不稳定,易被空气中氧气氧化生成铁离子;
④亚铁离子被氯气氧化生成铁离子,铁离子和硫氰化钾溶液反应生成络合物而显血红色;
⑤如果SCN-被过量的氯水氧化,向溶液中再加入KSCN或氯化铁溶液,根据溶液颜色是否变化确定乙猜想是否正确.
(2)①用于研碎药片的仪器是研钵;
②琥珀酸亚铁不溶于水,要检验亚铁离子应该加入酸将琥珀酸亚铁转化为可溶性的亚铁盐;
③亚铁离子不稳定,易被空气中氧气氧化生成铁离子;
④亚铁离子被氯气氧化生成铁离子,铁离子和硫氰化钾溶液反应生成络合物而显血红色;
⑤如果SCN-被过量的氯水氧化,向溶液中再加入KSCN或氯化铁溶液,根据溶液颜色是否变化确定乙猜想是否正确.
解答:
解:(1)亚铁盐不稳定,易被空气中氧气氧化生成铁盐,为防止亚铁盐被空气氧化而将补铁药剂通常都制成糖衣片,故答案为:防止二价铁被氧化为三价铁而变质;
(2)①用于研碎药片的仪器是研钵,故答案为:研钵;
②琥珀酸亚铁不溶于水,要检验亚铁离子应该加入酸将琥珀酸亚铁转化为可溶性的亚铁盐,可以用稀盐酸或稀硫酸,故答案为:稀硫酸或稀硫酸;
③亚铁离子不稳定,易被空气中氧气氧化生成铁离子,铁离子和KSCN生成络合物硫氰化铁而使溶液呈血红色,加入KSCN溶液的混合呈血红色,说明少量的Fe2+被空气中的氧气氧化,故答案为:少量的Fe2+被空气中的氧气氧化;
④亚铁离子被氯气氧化生成铁离子,铁离子和硫氰化钾溶液反应生成络合物而显血红色,离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-、Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN) 3),
故答案为:2Fe2++Cl2=2Fe3++2Cl-、Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN) 3);
⑤如果SCN-被过量的氯水氧化,向溶液中再加入KSCN或氯化铁溶液,根据溶液颜色是否变化确定乙猜想是否正确,其检验方法为:
取少量褪色后溶液,加入KSCN溶液;如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说明乙同学的猜想是不合理的;
或取少量褪色后溶液,加入FeCl3溶液;如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的;
故答案为:取少量褪色后溶液,加入KSCN溶液;如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说明乙同学的猜想是不合理的;
或取少量褪色后溶液,加入FeCl3溶液;如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的.
(2)①用于研碎药片的仪器是研钵,故答案为:研钵;
②琥珀酸亚铁不溶于水,要检验亚铁离子应该加入酸将琥珀酸亚铁转化为可溶性的亚铁盐,可以用稀盐酸或稀硫酸,故答案为:稀硫酸或稀硫酸;
③亚铁离子不稳定,易被空气中氧气氧化生成铁离子,铁离子和KSCN生成络合物硫氰化铁而使溶液呈血红色,加入KSCN溶液的混合呈血红色,说明少量的Fe2+被空气中的氧气氧化,故答案为:少量的Fe2+被空气中的氧气氧化;
④亚铁离子被氯气氧化生成铁离子,铁离子和硫氰化钾溶液反应生成络合物而显血红色,离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-、Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN) 3),
故答案为:2Fe2++Cl2=2Fe3++2Cl-、Fe3++SCN-=[Fe(SCN)]2+ (或Fe3++3SCN-=Fe(SCN) 3);
⑤如果SCN-被过量的氯水氧化,向溶液中再加入KSCN或氯化铁溶液,根据溶液颜色是否变化确定乙猜想是否正确,其检验方法为:
取少量褪色后溶液,加入KSCN溶液;如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说明乙同学的猜想是不合理的;
或取少量褪色后溶液,加入FeCl3溶液;如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的;
故答案为:取少量褪色后溶液,加入KSCN溶液;如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说明乙同学的猜想是不合理的;
或取少量褪色后溶液,加入FeCl3溶液;如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的.
点评:本题以亚铁离子、铁离子的转化为载体考查实验方案设计,明确物质的性质是解本题关键,根据物质的性质涉及实验,侧重考查实验操作、实验分析能力,知道铁离子、亚铁离子的检验方法及现象,题目难度中等.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
CH3COONa溶液中粒子浓度关系不正确的是( )
| A、c(Na+)>c(CH3COOH)>c(CH3COO-) |
| B、c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、c(Na+)=c(CH3COOH)+c(CH3COO-) |
| D、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
 在体积为VL的恒容密闭容器中盛有一定量的H2,通往Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.平衡时H2的体积分数与所加入Br2(g)的物质的量变化关系如图所示,下列说法正确的是( )
在体积为VL的恒容密闭容器中盛有一定量的H2,通往Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.平衡时H2的体积分数与所加入Br2(g)的物质的量变化关系如图所示,下列说法正确的是( )| A、由图可知:T1<T2 |
| B、a,b两点的反应速率:a>b |
| C、为了提高Br2的转化率,可采取将HBr及时移走 |
| D、T1时,随着Br2加入,平衡时Br2的转化率增大 |
一定条件下,对于反应X(g)+3Y(g)?2Z(g).若起始时浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z浓度分别为0.1mol?L-1、0.3mol?L-1和0.08mol?L-1,则下列判断不合理的是( )
| A、c1:c2=1:3 |
| B、c1的取值范围为0<c1<0.14 |
| C、X和Y的转化率相等 |
| D、平衡时,Y和Z的生成速率之比2:3 |
一定量某有机物X在O2中完全燃烧,生成了nmolCO2和nmolH2O,下列关于X的说法中正确的是( )
| A、X可能属于糖类物质 |
| B、X分子中一定含有不饱和键 |
| C、X分子中一定含有n个碳原子,2n个氢原子,但不能确定O原子数目 |
| D、X分子中若含有氧原子,则常温下X不可能是气体 |
高锰酸钾溶液在酸性条件下可以与亚铁离子反应,离子方程式如下(未配平):____MnO4+____Fe2++____H+═K2SO4+____Mn2++____Fe3++H2O,下列有关说法正确的是( )
| A、MnO4-和H+是氧化剂,Fe2+是还原剂 |
| B、H2O既是氧化物又是还原物 |
| C、每生成1mol水转移1.2mol的电子 |
| D、Fe2+的还原性强于Mn2+ |

 在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g)?pC(g)+qD(g).
在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g)?pC(g)+qD(g).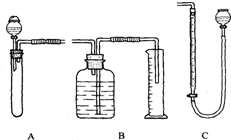 某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生成CO2体积的方法计算出样品中各组分的质量分数.为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计).如图是实验装置图,其中,B和C可供选择.请回答下列问题:
某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生成CO2体积的方法计算出样品中各组分的质量分数.为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计).如图是实验装置图,其中,B和C可供选择.请回答下列问题: