题目内容
CH3COONa溶液中粒子浓度关系不正确的是( )
| A、c(Na+)>c(CH3COOH)>c(CH3COO-) |
| B、c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| C、c(Na+)=c(CH3COOH)+c(CH3COO-) |
| D、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
考点:离子浓度大小的比较
专题:
分析:CH3COONa为强碱弱酸盐,水解呈碱性,结合电荷守恒、元素守恒解答该题.
解答:
解:CH3COONa为强碱弱酸盐,水解呈碱性,
A、CH3COONa溶液中CH3COO-)水解,但水解程度不大,所以c(CH3COO-)>c(CH3COOH),故A错误;
B、CH3COONa为强碱弱酸盐,水解呈碱性,所以有c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B正确;
C、根据元素守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),故C正确;
D、根据电荷守恒有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故D正确;
故选A.
A、CH3COONa溶液中CH3COO-)水解,但水解程度不大,所以c(CH3COO-)>c(CH3COOH),故A错误;
B、CH3COONa为强碱弱酸盐,水解呈碱性,所以有c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B正确;
C、根据元素守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),故C正确;
D、根据电荷守恒有c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故D正确;
故选A.
点评:本题主要考查了盐类的水解,难度不大,注重对基础知识的考查,答题时注意一般的盐类水解的程度都不大.

练习册系列答案
相关题目
下列实验不能获得成功的是( )
| A、用 浓溴水除去苯中混有的苯酚杂质 |
| B、淀粉与稀H2SO4充分反应后,加入适量新制Cu(OH)2溶液,加热产生红色沉淀 |
| C、用一种试剂稀硫酸可鉴别Na2S溶液,NaCl溶液、Na2SiO3溶液、Na2CO3溶液 |
| D、用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸杂质 |
 某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是( )
某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是( )A、断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl-
| ||||
| B、断开K2,闭合K1时,铜电极附近溶液变红 | ||||
| C、断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e-=2Cl- | ||||
| D、断开K1,闭合K2时,石墨电极作负极 |
下列叙述正确的是( )
| A、乙烯和苯都能使溴水褪色,故不能用溴水鉴别乙烯和苯 |
| B、HNO3能与苯、甲苯、甘油、纤维素等有机物发生重要反应,常用浓硫酸作催化剂 |
| C、仅用新制的氢氧化铜悬浊液一种试剂不能鉴别乙醇、乙醛、乙酸、葡萄糖溶液(必要时可加热〕 |
| D、苯与酸性KmnO4溶液混合振荡、静置分层,下层液体为无色 |
下列溶液一定呈碱性的是( )
| A、含有OH-的溶液 |
| B、c(OH-)>c(H+)的溶液 |
| C、c(OH-)>1×10-7mol?L-1的溶液 |
| D、滴入酚酞后显无色的溶液 |
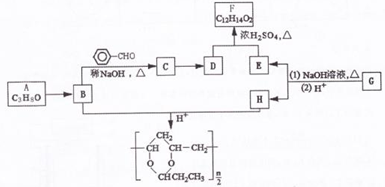
 +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)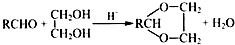
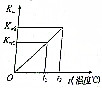 水的离子积常数Kw与温度t(℃)的关系如图所示:
水的离子积常数Kw与温度t(℃)的关系如图所示: