题目内容
11.下列哪一组元素的原子间反应容易形成离子键( )| 原子 | a | b | c | d | e | f | g |
| M层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| A. | a和c | B. | a和f | C. | d和g | D. | e和g |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属、碱土金属和第VIA族、第VIIA族元素之间易形成离子键,据此分析解答.
解答 解:活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,碱金属、碱土金属和第VIA族、第VIIA族元素之间易形成离子键,根据元素M电子层电子数知,a、b、c、d、e、f、g元素分别是Na、Mg、Al、Si、P、S、Cl元素,所以易形成离子键的是Na、Mg和S或Cl元素,A为Na、Al,B.形成NaCl,C.形成SiCl4,
D.形成PCl3,所以为离子化合物是氯化钠,
故选B.
点评 本题考查离子键判断,明确离子键概念及物质构成微粒即可解答,注意含有金属元素的物质中不一定含有离子键,如氯化铝,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
1.如图所示是四种分子结构的排列方式,其对应的化学式正确的是( )
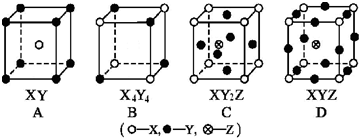

| A. | A | B. | B | C. | C | D. | D |
2.下列说法错误的是( )
| A. | I的原子半径大于Br,HI比HBr的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与氢键有关 |
19.已知某温度下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中不正确的是( )
| A. | 反应前,两溶液由水电离的H+浓度相同 | |
| B. | 当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-) | |
| C. | 若醋酸溶液加水稀释,溶液中各离子浓度与c(CH3COO-)/c(H+)均减小 | |
| D. | 相同温度,相同浓度的CH3COONH4 与 NaCl溶液,对水的电离程度的影响前者大于后者 |
16.下列说法不正确的是( )
| A. | 16O、18O互为同位素 | |
| B. | 金刚石和石墨互为同素异形体 | |
| C. | 分子式符合通式CnH2n+2且 n 值不同的两种烃互为同系物,而分子式符合通式CnH2n且 n 值不同的两种烃不一定互为同系物 | |
| D. | 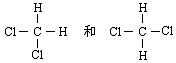 互为同分异构体 互为同分异构体 |
3.2010年上海世博会的主题是“城市,让生活更美好”.下列叙述中不正确的是( )
| A. | 世博会期间,处理废水时加入明矾可作为混凝剂以吸附水中的悬浮物杂质且有杀菌消毒的作用 | |
| B. | 世博会期间,利用可降解的“玉米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博会中国馆--“东方之冠”使用了大量钢筋混凝土,混凝土是混合物 | |
| D. | 世博停车场安装光电设施,可将阳光转化为电能以供应照明 |
20.某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.
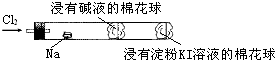
实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )

实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )
| A. | 钠着火燃烧产生苍白色火焰 | |
| B. | 反应生成的大量白烟是氯化钠晶体 | |
| C. | 管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 | |
| D. | 管右端棉球外颜色变化可判断氯气是否被碱液完全吸收 |
1.化学与社会、生活密切相关,下列说法正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 用活性炭为糖浆脱色和用臭氧漂白纸浆,原理相似 | |
| C. | 燃料电池的燃料都在负极发生氧化反应 | |
| D. | Fe3O4俗称铁红,常做红色油漆和涂料 |