题目内容
试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样按下图进行实验: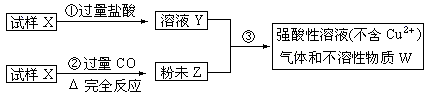
(1)请写出步聚③中发生的全部反应的离子方程式:____________________________________。
(2)要使试样X转变为粉末Z。除了CO外,还可以使用 。
| A.氢气 | B.焦炭 | C.氯气 | D.氧气 |
(1)Fe+2H+=Fe2++H2↑、Fe+Cu2+=Cu+Fe2+(各2分)
(2)AB(2分)(错无分,对1个得1分。共2分)
(3)0.625m或 m(3分)(带任何单位扣1分)
m(3分)(带任何单位扣1分)
解析试题分析:(1)氧化亚铁与氧化铜分别与盐酸反应生成氯化亚铁、氯化铜,因此溶液Y中含有亚铁离子、铜离子以及过量的盐酸。因为反应CuO+CO Cu+CO2,FeO+CO
Cu+CO2,FeO+CO Fe+CO2 ,所以固体粉末Z为Cu和Fe。铁能和铜离子发生置换反应,所以铁和铜离子发生的离子方程式为Fe+Cu2+=Cu+Fe2+;强酸性溶液E不含铜离子,且有气体F生成,所以铁与铜离子反应后铁过量,过量的铁还和酸反应,反应的离子方程式为Fe+2H+=Fe2++H2↑。
Fe+CO2 ,所以固体粉末Z为Cu和Fe。铁能和铜离子发生置换反应,所以铁和铜离子发生的离子方程式为Fe+Cu2+=Cu+Fe2+;强酸性溶液E不含铜离子,且有气体F生成,所以铁与铜离子反应后铁过量,过量的铁还和酸反应,反应的离子方程式为Fe+2H+=Fe2++H2↑。
(2)氢气与焦炭均具有还原性,能还原氧化亚铁与氧化铜,AB正确;氯气与氧气均具有强氧化性,不能还原金属氧化物,CD不正确,答案选AB。
(3)不溶物W为铜,铜有两部分来源,一部分是CO还原出的铜,一部分为铁与铜离子反应置换出的铜,所以以W的一半计算试样中的氧化铜的质量,则根据原子守恒可知
CuO~~~~~Cu
80 64 m m
m m
所以试样中氧化铜的质量为 m×
m× =
= m
m
考点:考查金属及其氧化物的性质、转化、物质含量的有关计算

 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案暗紫色化合物A具有绿色、高电压和高能量的特点,近年来引起了电化学界的高度重视。在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀,同时产生一种气体单质。某兴趣小组的同学对化合物A进行组成分析,确定A中仅含有O、K、Fe三种元素。取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)化合物A的化学式为 ;化合物A与H2O反应的离子方程式为 。
(2)化合物A还可作为一种“绿色高效多功能”水处理剂。原因是 。
(3)化合物A的制备还可通过氧化法,试写出在KOH存在条件下用次氯酸钾氧化氢氧化铁制备A的化学方程式 。
(4)目前,人们针对化合物A的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高化合物A水溶液稳定性的是
| A.亚硫酸钠 | B.KOH | C.醋酸 | D.Fe(NO3)3 |
铁单质及其化合物在生活、生产中应用广泛。请回答:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应是 。
(2)由于氧化性Fe3+>Cu2+氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是 。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是 (用离子方程式表示)。在使用时发现硫酸铁不能将酸性废水中的悬浮物沉降除去,其原因是 。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4十4CO 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是 。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是 (填字母)。
| | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 一定温度下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁表面形成致密氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |