题目内容
要除去混在氮气中的二氧化碳和一氧化碳得到纯净、干燥的氮气,正确方法是( )
| A、先通过石灰水,在通过灼热的氧化铜 |
| B、先通过常温下的氧化铜,再通过氢氧化钠 |
| C、先通过灼热的氧化铜,再通过氢氧化钠溶液,最后通过浓硫酸 |
| D、先通过灼热的铜,再通过石灰水 |
考点:物质分离、提纯的实验方案设计,物质的分离、提纯的基本方法选择与应用
专题:实验评价题
分析:CO具有还原性,二氧化碳能与碱反应,则利用CuO、NaOH来除杂,最后干燥即可得到纯净、干燥的氮气,以此来解答.
解答:
解:A.先通过石灰水,在通过灼热的氧化铜,生成二氧化碳,不能除杂,故A不选;
B.常温下CO与CuO不反应,不能除去CO,故B不选;
C.先通过灼热的氧化铜除去CO,再通过氢氧化钠溶液除去二氧化碳,最后通过浓硫酸干燥,可得到纯净、干燥的氮气,故C选;
D.CO与Cu不反应,不能除去CO,故D不选;
故选C.
B.常温下CO与CuO不反应,不能除去CO,故B不选;
C.先通过灼热的氧化铜除去CO,再通过氢氧化钠溶液除去二氧化碳,最后通过浓硫酸干燥,可得到纯净、干燥的氮气,故C选;
D.CO与Cu不反应,不能除去CO,故D不选;
故选C.
点评:本题考查物质分离、提纯的实验方案设计,为高频考点,把握物质的性质及分离方法为解答的关键,侧重除杂的考查,注意物质的性质差异及除杂原则,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
最高正化合价是它的负化合价的3倍的那一族元素是( )
| A、第ⅦA族 | B、第ⅥA族 |
| C、第ⅤA族 | D、第ⅢA族 |
一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相等.将1.0体积这种混合气体在氧气中完全燃烧,生成2.0体积的CO2和2.4体积的水蒸气(气体体积均在相同状况下测定),则混合气体中烷烃和烯烃的体积比为( )
| A、3:1 | B、1:3 |
| C、2:3 | D、3:2 |
下列有关物质性质的运用正确的是( )
| A、Na2O2与CO2反应放出的氧气:供矿山、坑道等地方呼吸之用 |
| B、纯碱:洗涤餐具上的油污 |
| C、三聚氰胺含有化合态的氮元素:补充人体蛋白质 |
| D、二氧化硫:用于制作馒头的增白剂 |
下列实验能成功的是( )
| A、加热硫酸、乙醇、氯化钠固体的混合物制氯乙烷 |
| B、福尔马林与苯酚的混合物,沸水浴加热制酚醛树脂 |
| C、氯乙烯加聚的生成物能使酸性KMnO4溶液褪色 |
| D、苯与浓溴水反应(Fe作催化剂)制溴苯 |
常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是( )
| A、pH>7,且 c(OH-)>c(Na+)>c(H+)>c(CH3COO-) |
| B、pH>7,且 c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C、pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D、pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
绿色化学又称环境友好化学,他的主要特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”.下列反应符合绿色化学这一特点的是( )
A、工业冶铁 Fe2O3+3CO
| ||||
| B、用生石灰制熟石灰 CaO+H2O═Ca(OH)2 | ||||
| C、实验室制二氧化碳2HCl+CaCO3═CaCl2+H2O+CO2↑ | ||||
| D、实验室制氢气 Zn+H2SO4═ZnSO4+H2↑ |
电解一定量的硫酸铜溶液的实验装置如图①,电解的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法正确的是( )
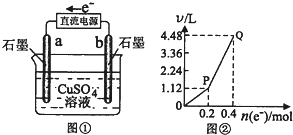

| A、开始时b电极有红色物质析出,而后有气泡产生 |
| B、a电极上的电子经溶液流向b极再流入直流电源 |
| C、曲线P~Q段表示产生H2和O2的体积比为1:2 |
| D、从开始到Q点收集到的混合气体中有0.1mol氧气 |
下列说法中正确的是( )
| A、凡能发生银镜反应的有机物一定是醛 |
| B、酸和醇发生的反应一定是酯化反应 |
| C、乙醇易溶于水是因为分子间形成了一种叫氢键的化学键 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |