题目内容
2.下列各组物质的性质比较中,不正确的是( )| A. | 原子半径:Na>P>O>F | B. | 稳定性:PH3<NH3<H2O<HF | ||
| C. | 碱性:KOH>NaOH>Mg(OH)2 | D. | 还原性:F->Cl->Br- |
分析 A.电子层越多,原子半径越大,电子层相同时,核电荷数越大,原子半径越小;
B.非金属性越强,氢化物的稳定性越强;
C.金属性越强,最高价氧化物对应水合物的碱性越强;
D.非金属性越强,阴离子的还原性越强.
解答 解:A.Na、P原子的比O、F多1个电子层,且原子序数Na<P、O<F,电子层越多,原子半径越大,电子层相同时,核电荷数越大,原子半径越小,则原子半径Na>P>O>F,故A正确;
B.非金属性P<N<O<F,非金属性越强,氢化物越稳定,则对应氢化物的稳定性:PH3<NH3<H2O<HF,故B正确;
C.金属性K>Na>Mg,则最高价氧化物对应水合物的碱性:KOH>NaOH>Mg(OH)2,故C正确;
D.非金属性F>Cl>Br,非金属性越强,对应阴离子的还原性越弱,则阴离子的还原性:F-<Cl-<Br-,故D错误;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,明确元素周期律内容为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
10.在Na+浓度为0.9mol•L-1的某澄清溶液中,还可能含有下表中的若干种离子:
取该溶液100ml进行如下实验(气体体积在标准状况下测定):
I.向该溶液中加入足量稀HCl,产生白色沉淀并放出1.12L气体
II.将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称得固体质量为3.6g
III.在II的滤液中滴加BaCl2溶液,无明显现象
下列说法不正确的是( )
| 阳离子 | K+、Ag+、Mg2+、Ba2+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42- |
I.向该溶液中加入足量稀HCl,产生白色沉淀并放出1.12L气体
II.将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称得固体质量为3.6g
III.在II的滤液中滴加BaCl2溶液,无明显现象
下列说法不正确的是( )
| A. | K+一定存在,且c(K+)≤1.3mol•L-1 | |
| B. | 实验I能确定一定不存在的离子是Ag+、Mg2+、Ba2+ | |
| C. | 实验I中生成沉淀的离子方程式为SiO32-+2H+=H2SiO3↓ | |
| D. | 实验III能确定一定不存在SO42- |
13.制备下列气体过程中,净化除杂的有关操作(括号内是杂质),正确的是( )
| A. | CO2(CO):气体通过灼热的CuO | |
| B. | Cl2(SO2):通入盛有品红溶液的洗气瓶 | |
| C. | NO(NO2):通过水洗,再干燥后,用向下排空气法收集 | |
| D. | H2(CO2):依次通过盛有氢氧化钠溶液和浓硫酸的洗气瓶 |
10.下列物质中,属于电解质的是( )
| A. | Fe | B. | H2SO4 | C. | CH4 | D. | 酒精 |
17.用NA表示阿佛加德罗常数的值,下列说法正确的是( )
| A. | 乙烯和环丙烷(C3H6)组成的28g混合气体中含有2 NA个碳原子 | |
| B. | 7.8 g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 | |
| C. | 标准状况下,2.24L已烷含有分子的数目为0.1NA | |
| D. | 1molCH4O中含有C-H键的数目为4NA |
7.下列措施中,能加快化学反应速率的是( )
| A. | 将食物储存在冰箱里 | |
| B. | 用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 | |
| C. | 往H2O2溶液中加入几滴FeCl3溶液 | |
| D. | 用纯锌代替粗锌与1 mol/L H2SO4溶液反应 |
14.某小组利用H2O2溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如下的方案.
(1)已知反应后H2O2转化为O2逸出,KMnO4转化为MnSO4,请写出该反应的离子方程式5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O.
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.01 mol•L-1•min-1.
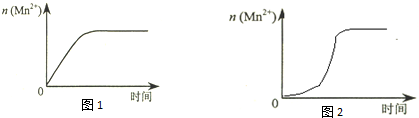
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.
①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
③若该小组同学提出的假设成立,应观察到的现象是与实验①比较,溶液褪色所需时间短(或所用时间(t)小于40s).
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.01 mol•L-1•min-1.
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.

①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | 再向试管中加入少量固体 | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | |||
| ④ | 0.10 | 2.0 | 0.010 | 4.0 | 25 | |
11.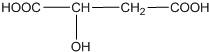 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能发生消去反应 | |
| D. | 1mol苹果酸与金属钠作用,最多能产生3mol氢气 |
12.能正确表示下列化学反应的离子方程式是( )
| A. | 稀盐酸与铁粉反应:Fe+2H+=Fe2++H2↑ | |
| B. | 碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ | |
| C. | 锌片插入硝酸银溶液中:Zn+2Ag+=Zn2++2Ag | |
| D. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |