题目内容
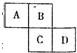 如图是元素周期表的一部分.A、B、C、D均为短周期元素,其中C元素原子核外电子总数是其最外层电子数的3倍,则下列说法中不正确的是( )
如图是元素周期表的一部分.A、B、C、D均为短周期元素,其中C元素原子核外电子总数是其最外层电子数的3倍,则下列说法中不正确的是( )| A、B元素的氢化物的稳定性低于C元素的氢化物的稳定性 |
| B、B元素的氢化物水溶液滴加酚酞试液变红 |
| C、最高价氧化物对应的水化物的酸性:D>C |
| D、阴离子半径从大到小的排列顺序为:C>D>B |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素A、B、C、D在周期表中位置,可知A、B处于第二周期,C、D处于第三周期,C元素原子核外电子总数是其最外层电子数的3倍,令最外层电子数为x,则2+8+x=3x,解得x=5,故C为P元素,可推知A为C元素、B为N元素、D为S元素.
A.同主族自上而下非金属性减弱,氢化物稳定性减弱;
B.氨水溶液呈碱性;
C.同周期自左而右非金属性增强,最高价含氧酸的酸性增强;
D.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大.
A.同主族自上而下非金属性减弱,氢化物稳定性减弱;
B.氨水溶液呈碱性;
C.同周期自左而右非金属性增强,最高价含氧酸的酸性增强;
D.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大.
解答:
解:由短周期元素A、B、C、D在周期表中位置,可知A、B处于第二周期,C、D处于第三周期,C元素原子核外电子总数是其最外层电子数的3倍,令最外层电子数为x,则2+8+x=3x,解得x=5,故C为P元素,可推知A为C元素、B为N元素、D为S元素,
A.非金属性N>P,故氢化物稳定性NH3>PH3,故A错误;
B.氨水溶液呈碱性,滴加酚酞试液变红,故B正确;
C.非金属性Cl>P,故最高价氧化物对应的水化物的酸性:高氯酸>磷酸,故C正确;
D.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:P3->S2->N3-,故D正确,
故选A.
A.非金属性N>P,故氢化物稳定性NH3>PH3,故A错误;
B.氨水溶液呈碱性,滴加酚酞试液变红,故B正确;
C.非金属性Cl>P,故最高价氧化物对应的水化物的酸性:高氯酸>磷酸,故C正确;
D.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:P3->S2->N3-,故D正确,
故选A.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,侧重对元素周期律的考查,难度不大.

练习册系列答案
相关题目
分类是化学研究的重要方法,下列各组物质的分类正确的是( )
| A、同位素:D2、H2、T2 |
| B、含极性键、由分子构成的化合物:CO2、CCl4、NH3 |
| C、非电解质:NH3、C2H5OH、Cl2 |
D、同系物: |
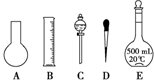
下列图所示的实验操作中,不正确的是( )
A、 滴加液体药品 |
B、 过滤 |
C、 稀释浓硫酸 |
D、 读取液体的体积 |
在25℃,某稀溶液中由水电离产生的c(H+) 为10-13mol/L,下列有关溶液的叙述正确的是( )
| A、该溶液一定呈酸性 |
| B、该溶液一定呈碱性 |
| C、该溶液的pH可能约为1 |
| D、该溶液的pH可能约为13,也可能为1 |
不能用于判断HA是弱电解质(弱酸)的依据是( )
| A、浓度相等的HCl与HA,跟锌反应生成氢气的速率HCl比HA快 |
| B、pH相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多 |
| C、浓度相等的NaCl与NaA两溶液,前者是中性而后者为碱性 |
| D、浓度相等体积相同的HCl与HA两溶液与足量氢氧化钠溶液反应时,消耗的氢氧化钠一样多 |
常温下,下列有关叙述正确的是学( )
| A、NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6mol/L |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液,其pH可能等于或大于7 |
| D、10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积(假设混合后的体积是两溶液体积之和)V(总)≥20mL |
下列有关化学与生活、工业的叙述中,正确的是( )
| A、工业上生产水泥、玻璃、陶瓷,均需要用石灰石为原料 |
| B、石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能 |
| C、面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物 |
| D、地沟油由于混有一些对人体有害的杂质而不能食用,可加工制成生物柴油,生物柴油的成分与从石油中提取的柴油成分不同 |
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: