题目内容
分类是化学研究的重要方法,下列各组物质的分类正确的是( )
| A、同位素:D2、H2、T2 |
| B、含极性键、由分子构成的化合物:CO2、CCl4、NH3 |
| C、非电解质:NH3、C2H5OH、Cl2 |
D、同系物: |
考点:同位素及其应用,极性键和非极性键,电解质与非电解质,芳香烃、烃基和同系物
专题:物质的分类专题
分析:A.有相同质子数,不同中子数的原子互为同位素;
B.极性键:不同种原子形成的共价键;
C.非电解质:在熔融状态和水溶液中都不能导电的化合物;
D.结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物.
B.极性键:不同种原子形成的共价键;
C.非电解质:在熔融状态和水溶液中都不能导电的化合物;
D.结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物.
解答:
解:A.D2、H2、T2是由氢的同位素原子构成的氢分子,不能互为同位素,故A错误;
B.CO2是由二氧化碳分子构成的化合物,含有C-O极性键;CCl4是由四氯化碳分子构成的化合物,含有C-Cl极性键;NH3是由氨气分子构成的化合物,含有N-H极性键,故B正确;
C.NH3、C2H5OH为非电解质;氯气是单质,既不是电解质也不是非电解质,故C错误;
D.苯酚、苯酚与苯乙醇结构不同,故不能互为同系物,故D错误;
故选B.
B.CO2是由二氧化碳分子构成的化合物,含有C-O极性键;CCl4是由四氯化碳分子构成的化合物,含有C-Cl极性键;NH3是由氨气分子构成的化合物,含有N-H极性键,故B正确;
C.NH3、C2H5OH为非电解质;氯气是单质,既不是电解质也不是非电解质,故C错误;
D.苯酚、苯酚与苯乙醇结构不同,故不能互为同系物,故D错误;
故选B.
点评:本题考查同位素、极性键、非电解质及同系物的判断,难度不大.要注意基础知识的积累.

练习册系列答案
相关题目
将铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是( )
| A、硫酸 | B、磷酸 |
| C、硝酸锌 | D、氯化铜 |
在2molNa2SO4中,含有Na+的数目是( )
| A、1.204×1024 |
| B、1.204×1023 |
| C、2.408×1024 |
| D、2.408×1023 |
下列物质在一定条件下可以使紫色石蕊试液褪色,且漂白原理相同的是( )
①次氯酸钠 ②活性炭 ③浓硝酸 ④稀硝酸 ⑤过氧化钠.
①次氯酸钠 ②活性炭 ③浓硝酸 ④稀硝酸 ⑤过氧化钠.
| A、①③⑤ | B、①④⑤ |
| C、②④⑤ | D、①③④ |
标准状况下,体积相同的下列四组物质,分子数相同的一组是( )
| A、Cl2、CO |
| B、CO、CCl4 |
| C、CO、C |
| D、H2O、CO2 |
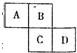 如图是元素周期表的一部分.A、B、C、D均为短周期元素,其中C元素原子核外电子总数是其最外层电子数的3倍,则下列说法中不正确的是( )
如图是元素周期表的一部分.A、B、C、D均为短周期元素,其中C元素原子核外电子总数是其最外层电子数的3倍,则下列说法中不正确的是( )| A、B元素的氢化物的稳定性低于C元素的氢化物的稳定性 |
| B、B元素的氢化物水溶液滴加酚酞试液变红 |
| C、最高价氧化物对应的水化物的酸性:D>C |
| D、阴离子半径从大到小的排列顺序为:C>D>B |
下列实验对应的结论不正确的是( )
A、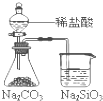 能证明非金属性Cl>C>Si |
B、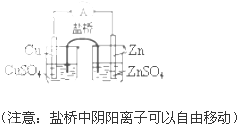 能组成Zn、Cu原电池 |
C、 颜色深浅不同说明反应2NO2═N2O4;△H<0 |
D、 白色沉淀为BaSO4 |