题目内容
将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应 NO2(g)+CO(g) CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
 CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )A.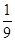 | B. | C. | D.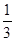 |
C
试题分析: NO2(g)+CO(g) CO2(g)+NO(g)
CO2(g)+NO(g)
起始量(mol) 1 1 0 0
转化量(mol) 0.5 0.5 0.5 0.5
平衡量(mol) 0.5 0.5 0.5 0.5
则平衡常数K=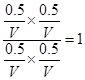
NO2(g)+CO(g) CO2(g)+NO(g)
CO2(g)+NO(g)
起始量(mol) 1 2 0 0
转化量(mol) x x x x
平衡量(mol) (1-x)(2-x) x x
则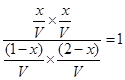
解得x=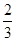
所以反应达到化学平衡时,混合气体中CO2的体积分数是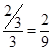
答案选C。
点评:该题是基础性试题的考查,难度不大。该题学生需要明确的是做这类试题的基本要求,即在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。该题有利于培养学生的规范答题能力。
试题分析: NO2(g)+CO(g)
 CO2(g)+NO(g)
CO2(g)+NO(g)起始量(mol) 1 1 0 0
转化量(mol) 0.5 0.5 0.5 0.5
平衡量(mol) 0.5 0.5 0.5 0.5
则平衡常数K=
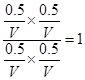
NO2(g)+CO(g)
 CO2(g)+NO(g)
CO2(g)+NO(g)起始量(mol) 1 2 0 0
转化量(mol) x x x x
平衡量(mol) (1-x)(2-x) x x
则
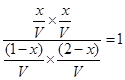
解得x=
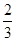
所以反应达到化学平衡时,混合气体中CO2的体积分数是
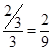
答案选C。
点评:该题是基础性试题的考查,难度不大。该题学生需要明确的是做这类试题的基本要求,即在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。该题有利于培养学生的规范答题能力。

练习册系列答案
相关题目
 CO(NH2)2(l) + H2O (l) ΔH < 0 。回答下列问题:
CO(NH2)2(l) + H2O (l) ΔH < 0 。回答下列问题: NH2COONH4(s) ΔH1< 0
NH2COONH4(s) ΔH1< 0 CO(NH2)2(l)+ H2O (l) ΔH 2> 0
CO(NH2)2(l)+ H2O (l) ΔH 2> 0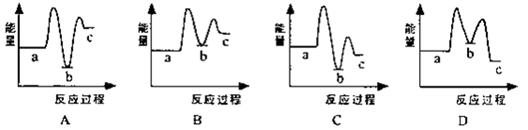
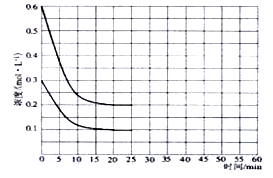
 2Z(g);若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是
2Z(g);若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是 
 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( ) 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据右图可得出的判断结论正确的是 
 2HI(g) ②C(s)+H2O(g)
2HI(g) ②C(s)+H2O(g) 2 NH3的说法不正确的是( )
2 NH3的说法不正确的是( ) C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是