题目内容
(1)室温时,氢氧化钙的溶度积KSP=4.7×10-6,室温时将9mL0.02mol?L-1的氯化钙溶液与1mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中 沉淀析出(填“有”或“无”).
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4?yH2O),做如下实验:将固体加热,经测量剩余固体质量随时间变化如图所示.

则x:y= .t2~t3时间段固体的化学式为 .t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色.则该时间所发生反应的化学方程式为 .
(2)某校课外活动小组为测定已部分脱水的生石膏的组成(xCaSO4?yH2O),做如下实验:将固体加热,经测量剩余固体质量随时间变化如图所示.

则x:y=
考点:探究物质的组成或测量物质的含量,难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:(1)如果c(Ca2+).c2(OH-)<KSP就没有沉淀析出,如果c(cCa2+).c2(OH-)>KSP就有沉淀析出;
(2)从D点开始,t5~t6时间段固体质量减轻的原因是产生了两种气体,说明该点的固体为硫酸钙,则硫酸钙的物质的量=
=0.02mol,水的物质的量=
=0.03mol,据此判断该物质的化学式;
t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,说明生成二氧化硫气体,根据元素得失电子知,还有氧气生成,据此书写方程式.
(2)从D点开始,t5~t6时间段固体质量减轻的原因是产生了两种气体,说明该点的固体为硫酸钙,则硫酸钙的物质的量=
| 2.72g |
| 136g/mol |
| (3.26g-2.72g) |
| 18g/mol |
t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,说明生成二氧化硫气体,根据元素得失电子知,还有氧气生成,据此书写方程式.
解答:
解:(1)c(Ca2+)=
=0.018mol/L,cc(OH-)=
=0.01mol/L,则c(Ca2+).c2(OH-)=0.018×0.01×0.01=1.8×10-6<KSP,所以没有沉淀析出,
故答案为:无;
(2)从D点开始,t5~t6时间段固体质量减轻的原因是产生了两种气体,说明该点的固体为硫酸钙,则硫酸钙的物质的量=
=0.02mol,水的物质的量=
=0.03mol,则硫酸钙和水的物质的量之比等于其个数之比=0.02mol:0.03mol=2:3;
t2~t3时间段,固体中水的物质的量为:
=0.01mol,则硫酸钙和水的物质的量之比等于其个数之比=0.02mol:0.01mol=2:1,所以该物质的化学式为:2CaSO4?H2O或CaSO4?
H2O;
t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,说明生成二氧化硫气体,根据元素得失电子知,还有氧气生成,1,12g可能为氧化钙的质量,物质的量为:
=0.02mol,和0.02molCaSO4分解生成0.02mol氧化钙正好吻合,所以该反应方程式为:2CaSO4
2CaO+2SO2↑+O2↑,
故答案为:2:3;2CaSO4?H2O或CaSO4?
H2O;2CaSO4
2CaO+2SO2↑+O2↑.
| 0.02mol/L×9mL |
| 10mL |
| 0.1mol/L×1mL |
| 10mL |
故答案为:无;
(2)从D点开始,t5~t6时间段固体质量减轻的原因是产生了两种气体,说明该点的固体为硫酸钙,则硫酸钙的物质的量=
| 2.72g |
| 136g/mol |
| (3.26g-2.72g) |
| 18g/mol |
t2~t3时间段,固体中水的物质的量为:
| 2.90g-2.72g |
| 18g/mol |
| 1 |
| 2 |
t5~t6时间段固体质量减轻的原因是产生了两种气体,其中一种能使品红溶液褪色,说明生成二氧化硫气体,根据元素得失电子知,还有氧气生成,1,12g可能为氧化钙的质量,物质的量为:
| 1.12g |
| 56g/mol |
| ||
故答案为:2:3;2CaSO4?H2O或CaSO4?
| 1 |
| 2 |
| ||
点评:本题考查了溶度积常数、物质的分解等知识点来分析解答,难点是(2),明确曲线变化趋势及拐点含义即可解答,知道每一步发生的反应,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
短周期元素A、B,若A离子与B离子电子层结构相同,且A离子半径大于B离子半径,则下列说法一定正确的是( )
| A、原子半径A<B |
| B、电负性A<B |
| C、元素A、B不同周期 |
| D、A原子序数小于B原子序数 |
下列有关化学用语书写正确的是( )
①蔗糖的最简式是CH2O
②次氯酸的结构式:H-Cl-O
③苯甲醇的结构简式: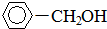
④甲烷分子的比例模型:
⑤S2-的电子排布图为:1s22s22p63s23p6
⑥原子核内有10个中子的氧离子:
O2-.
①蔗糖的最简式是CH2O
②次氯酸的结构式:H-Cl-O
③苯甲醇的结构简式:
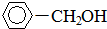
④甲烷分子的比例模型:

⑤S2-的电子排布图为:1s22s22p63s23p6
⑥原子核内有10个中子的氧离子:
18 8 |
| A、②③⑥ | B、③⑥ |
| C、①③⑤⑥ | D、①②③④⑤⑥ |
“稀土”是我国宝贵的战略资源,国家即将控制其出口.
Sm 与
Sm是稀土元素,下列有关说法不正确的是( )
144 62 |
150 62 |
A、
| ||||
B、
| ||||
C、
| ||||
D、据
|
某溶液100mL,其中c(H2SO4)为0.3 mol/L,c(HNO3)为0.4 mol/L,若在该溶液中投入1.92g铜粉微热,充分反应后,所得溶液中Cu2+的物质的量浓度为(假设反应前后溶液的体积不变)( )
| A、0.15mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
将过量的CO2分别通入下列溶液中,最终有沉淀析出的是( )
| A、CaCl2溶液 |
| B、饱和Na2CO3溶液 |
| C、Ca(ClO)2溶液 |
| D、Ca(OH)2溶液 |