题目内容
20. 甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.
甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色.(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验.取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
(3)资料显示:SCN -的电子式为
 .甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究.
.甲同学猜想SCN-可能被Cl2氧化了,他进行了如下研究.①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
②甲同学通过实验证明了SCN-中氮元素转化为NO3-,已知SCN-中碳元素没有被氧化,若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
分析 探究Cl2与FeCl2和KSCN混合溶液的反应,Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化铁溶液,呈红色,向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色,A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,应当是氢氧化铁固体,根据SCN-的电子式为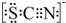 可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素.
可知,SCN-中碳显+4价,硫显-2价,氮显-3价,碳已经是最高正价了,不能再被氧化,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素.
(1)B装置是用来吸收氯气尾气的,根据元素守恒和电荷守恒可以写出离子方程式;
(2)A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,应当是氢氧化铁固体,所以原溶液中应当有Fe3+;
(3)①加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素;
②SCN-与Cl2反应的化学方程式可以计算出电子转移的物质的量.
解答 解:(1)B装置是用来吸收氯气尾气的,根据元素守恒和电荷守恒可以写出离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
(2)A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,应当是氢氧化铁固体,所以原溶液中应当有Fe3+,
故答案为:Fe3+;
(3)①加入用盐酸酸化的BaCl2溶液,产生白色沉淀,说明白色沉淀为硫酸钡,即溶液中有硫酸根离子,其中硫显+6价,而原来SCN-中硫显-2价,所以被氧化的元素为硫元素,
故答案为:硫元素;
②SCN-与Cl2反应生成硫酸根和硝酸根还有二氧化碳,所以它们反应的化学方程式为:SCN-+8Cl2+9H2O=NO3-+SO42-+CO2+Cl-+18H+,此反应中电子转移数目为16,即由方程式可知每生成1mol二氧化碳要转移16mol电子,
故答案为:16.
点评 本题是实验方案的综合题,综合性较强,其中涉及到了离子的检验、氧化还原的离子方程式的书写、化学计算等知识点,解题的关键是要掌握元素化合物的基础知识及实验基本操作要求,题目难度中等.

| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 乙醇与甲醚、分子式均为C2H6O,二者互为同分异构体 | |
| D. | 乙烯与聚乙烯不能互称为同系物 |

| A. | 苯氧乙酸与菠萝酯互为同系物 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| D. | 步骤(2)产物中残留的烯丙醇可用溴水检验 |
| A. | 通入大量O2 | B. | 减小体系压强 | C. | 移去部分SO3 | D. | 降低体系温度 |
| A. | 6 mol•L-1 | B. | 6.75 mol•L-1 | C. | 6.25 mol•L-1 | D. | 5 mol•L-1 |
| A. | CH3-CH=CH2与 | B. |  与 与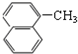 | ||
| C. |  与 与 | D. | CH3CH2Cl与CH3CHCl-CH2Cl |
 CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.
CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.