题目内容
关于下列各实验装置的叙述中,不正确的是( )
A、 如图可用于实验室制取少量NH3或O2 |
B、 可用从a处加水的方法检验如图装置的气密性 |
C、 实验室可用如图的方法收集Cl2 |
D、 利用如图装置制硫酸和氢氧化钠,其中b为阴离子交换膜、c为阳离子交换膜 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.利用装置,可用浓氨水和碱石灰制备氨气,用过氧化氢和二氧化锰制备氧气;
B.从a处加水,如左边液面不发生变化,可证明气密性良好;
C.氯气比空气密度大;
D.电解硫酸钠溶液,阴离子向阳极移动,在阳极上生成氧气和硫酸,阳离子向阴极移动,在阴极上生成氢气和氢氧化钠,以此选取离子交换膜.
B.从a处加水,如左边液面不发生变化,可证明气密性良好;
C.氯气比空气密度大;
D.电解硫酸钠溶液,阴离子向阳极移动,在阳极上生成氧气和硫酸,阳离子向阴极移动,在阴极上生成氢气和氢氧化钠,以此选取离子交换膜.
解答:
解:A.图为固体和液体不加热反应装置,故可用于实验室制取少量NH3或O2,故A正确;
B.从a处加水的方法可以密封一段气体,故可以检验图②装置的气密性,故B正确;
C.氯气比空气密度大,从短管进是错误的,故C错误;
D.左侧为阳极室,氢氧根离子放电后生成硫酸,故b为阴离子交换膜允许硫酸根离子通过、右侧阴极室,氢离子放电生成氢氧化钠,故c为阳离子交换膜允许钠离子通过,故D正确.
故选C.
B.从a处加水的方法可以密封一段气体,故可以检验图②装置的气密性,故B正确;
C.氯气比空气密度大,从短管进是错误的,故C错误;
D.左侧为阳极室,氢氧根离子放电后生成硫酸,故b为阴离子交换膜允许硫酸根离子通过、右侧阴极室,氢离子放电生成氢氧化钠,故c为阳离子交换膜允许钠离子通过,故D正确.
故选C.
点评:本题较为综合,涉及多个方面的知识,有对新教材《实验化学》的强调,实验装置的熟悉度,电解池装置中离子交换膜的知识点,题目难度中等,注意把握离子交换膜的判断.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、所有的蛋白质、多糖及油脂均可以水解 |
| B、氢键在形成蛋白质的二级结构和DNA的双螺旋结构中起着关键作用 |
| C、光导纤维、玻璃纤维和光电池板的主要成份均是二氧化硅 |
| D、为了减缓月饼等富脂食品变质,可在包装内放入小包装的还原铁粉 |
将0.2mol/L的醋酸钠溶液与0.1mol/L盐酸等体积混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
| A、c (Ac-)>c (Na+)>c (H+)>c (HAc) |
| B、c (Na+)+c (H+)=c (Ac-)+c (Cl-) |
| C、c (Ac-)=c (Cl-)>c (H+)>c (HAc) |
| D、c (Ac-)>c (Cl-)>c (HAc)>c(H+) |
如图为浓度各为0.1mol/L的酸HA和碱BOH的溶液中,溶质分子浓度随pH值的改变而变化的情况.下列说法中不正确的是( )
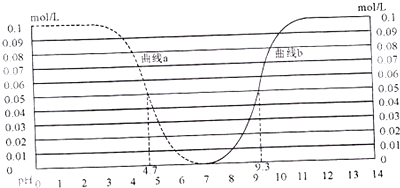

| A、曲线a代表酸HA,曲线b代表碱BOH | ||
B、在0.1mol/L的BOH溶液中,但溶液的pH从8逐渐变为11时,
| ||
| C、在0.1mol/L的NaA溶液中,若通过加少量纯HA改变溶液pH时,一定有:c(Na+)-c(OH-)=c(A-)-c(H+) | ||
| D、用等物质的量浓度的NaOH溶液和盐酸分别滴定等浓度等体积的酸HA和BOH溶液时,所消耗的NaOH溶液和盐酸的体积相同 |
下列说法正确的是( )
| A、在酸碱中和滴定实验中可用传感技术绘制中和滴定曲线 |
| B、向试管中加入4mL 0.1mol?L-1K2Cr2O7溶液,再滴加数滴1 mol?L-1NaOH溶液,溶液颜色由黄色变为橙色 |
| C、在制备硝酸钾晶体的实验中,趁热过滤时,承接滤液的小烧杯中先加入2mL的水,以防过滤时烧杯中的硝酸钾晶体过早析出 |
| D、蒸馏时温度计水银球插在蒸馏烧瓶支管口的下方位置,将收集到高沸点馏分 |
下列各条件下一定能共存的离子组是( )
| A、某无色溶液中:NH4+、Na+、Cl-、MnO4- |
| B、由水电离出的c(H+)═1×10-13mol?L-1的溶液中:Na+、K+、SO42-、HCO3- |
| C、在c(H+)═1×10-13mol?L-1的溶液中:Na+、AlO2-、SO42-、NO3- |
| D、在FeSO4的溶液中:K+、Na+、Cl-、NO3- |
下列离子或分子在给定的条件下一定能大量共存的是( )
| A、由水电离的c(H+)=1×10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B、使甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| C、pH=10的溶液中:Na+、Cl-、SO42-、NO3- |
| D、含有CO32-的溶液中:K+、C6H5OH、Cl2、SO42- |
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入 0.1mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1molAg.则下列结论中不正确的是( )
| A、反应后溶液中Cu2+与Fe2+的物质的量之比为1:2 |
| B、氧化性:Ag+>Fe3+>Cu2+>Zn2+ |
| C、含Fe3+的溶液可腐蚀铜板 |
| D、1molFe可还原1molFe3+ |
 ⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.
⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.