题目内容
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1.8g水中含有中子数为NA |
| B、标准状况下,22.4L CO和C2H4混合气体的总分子数为NA,质量为28g |
| C、1L 0.1mol/L-1稀盐酸中,HCl分子数目为0.1NA |
| D、常温常压下,1mol甲基所含电子数为10NA |
考点:阿伏加德罗常数
专题:
分析:A、1mol水含8mol中子;
B、CO和C2H4的摩尔质量均为28g/mol;
C、盐酸溶液中,无HCl分子;
D、根据甲基不显电性来分析.
B、CO和C2H4的摩尔质量均为28g/mol;
C、盐酸溶液中,无HCl分子;
D、根据甲基不显电性来分析.
解答:
解:A、1.8g水的物质的量为0.1mol,而1mol水含8mol中子,故0.1mol水含0.8mol中子,个数为0.8NA个,故A错误;
B、标况下,22.4LCO和C2H4的混合气体的物质的量为1mol,故分子数为N=n?NA=NA个,而CO和C2H4的摩尔质量均为28g/mol,故混合气体的质量m=nM=1mol×28g/mol=28g,故B正确;
C、HCl溶于水得盐酸,而HCl溶于水后完全电离,故在盐酸溶液中,无HCl分子,故C错误;
D、甲基不显电性,故1mol-CH3含9mol电子,个数为9NA,故D错误;
故选B.
B、标况下,22.4LCO和C2H4的混合气体的物质的量为1mol,故分子数为N=n?NA=NA个,而CO和C2H4的摩尔质量均为28g/mol,故混合气体的质量m=nM=1mol×28g/mol=28g,故B正确;
C、HCl溶于水得盐酸,而HCl溶于水后完全电离,故在盐酸溶液中,无HCl分子,故C错误;
D、甲基不显电性,故1mol-CH3含9mol电子,个数为9NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列对有机物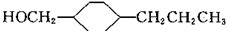 的说法,正确的是( )
的说法,正确的是( )
 的说法,正确的是( )
的说法,正确的是( )| A、属于芳香族化合物 |
| B、属于酚类物质 |
C、不能由有机物 催化加氢得到 催化加氢得到 |
D、能由有机物 催化加氢得到 催化加氢得到 |
 如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、1molH2中的化学键断裂时需要吸收436kJ能量 |
| B、2molHCl分子中的化学键形成时要释放862kJ能量 |
| C、稳定性:H2(g)>HCl(g) |
| D、此反应的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-248kJ/mol |
下列叙述正确的是( )
| A、溶液和胶体的本质区别是有无丁达尔效应 |
| B、玻璃、水泥和光导纤维的主要成分都是硅酸盐 |
| C、NaCl和NH4Cl中所含化学键种类相同 |
| D、熵增大的自发反应,可能是吸热反应 |
下列有关化学用语使用正确的是( )
| A、乙酸、葡萄糖、淀粉的最简式均为CH2O |
B、羧基的电子式为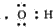 |
C、乙醇分子的比例模型为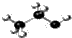 |
D、2-羧基丁酸的键线式为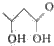 |
下列反应的方程式书写正确的( )
A、氯乙烷消去反应制乙烯:CH3CH2Cl
| |||
B、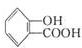 +2Na2CO3→ +2Na2CO3→ +2NaHCO3 +2NaHCO3 | |||
| C、苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |||
D、甲醛溶液中加入足量的银氨溶液并水浴加热:HCHO+2[Ag(NH3)2]+2OH-
|
碳纳米管和石墨烯(由石墨剥离的层状结构)经低温处理,获得了一种“最轻材料”.该材料具有超强的吸附能力,还有望成为理想的储能保温材料.下列有关说法正确的是( )
| A、石墨烯属于共价化合物 |
| B、该材料吸油过程为物理变化 |
| C、碳纳米管和石墨烯互为同位素 |
| D、碳纳米属于胶体分散系 |
将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是( )
| A、Ca(OH)2的溶解度、溶剂的质量 |
| B、溶液中溶质的质量分数 |
| C、溶液的质量、水的电离平衡 |
| D、溶液中Ca2+的数目 |
