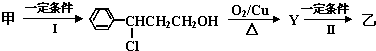题目内容
下列叙述正确的是( )
| A、溶液和胶体的本质区别是有无丁达尔效应 |
| B、玻璃、水泥和光导纤维的主要成分都是硅酸盐 |
| C、NaCl和NH4Cl中所含化学键种类相同 |
| D、熵增大的自发反应,可能是吸热反应 |
考点:胶体的重要性质,硅酸盐工业,化学键,吸热反应和放热反应
专题:
分析:A.溶液与胶体的本质不同的原因是微粒直径不同,胶体的微粒直径在1-100nm之间,溶液的微粒直径小于1-100nm;
B.光导纤维的主要成分是二氧化硅;
C.离子键,共价键是不同的化学键;
D.△H-T△S<0判断.
B.光导纤维的主要成分是二氧化硅;
C.离子键,共价键是不同的化学键;
D.△H-T△S<0判断.
解答:
解:A.溶液与胶体的本质不同的原因是微粒直径不同,故A错误;
B.光导纤维的主要成分是二氧化硅,二氧化硅不是硅酸盐,故B错误;
C.NaCl中只有离子键,NH4Cl中有离子键也有共价键(N与H的),故C错误;
D.熵增大的自发反应,即△S>0,△H-T△S<0,可能△H<0,故D正确.
故选D.
B.光导纤维的主要成分是二氧化硅,二氧化硅不是硅酸盐,故B错误;
C.NaCl中只有离子键,NH4Cl中有离子键也有共价键(N与H的),故C错误;
D.熵增大的自发反应,即△S>0,△H-T△S<0,可能△H<0,故D正确.
故选D.
点评:本题考查溶液和胶体的本质区别、硅酸盐、危险品标志、化学键,难度不大,注意NH4Cl中有离子键也有共价键.

练习册系列答案
相关题目
已知热化学方程式:2H2(g)+O2(g)=2H2O(g)△H1=-483.6kJ/mol.则对于热化学方程式:2H2O(l)=2H2(g)+O2(g)△H2=b,下列说法正确的是( )
| A、热化学方程式中化学计量数表示分子个数 |
| B、该反应的△H2=+483.6 kJ/mol |
| C、△H2<△H1 |
| D、△H2>△H1 |
已知2KmnO4+16HCI=2KC1+2MnCI2+5C12↑+8H20;K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O
MnO2+4HCl═MnCl2+Cl2↑+2H2O ;其中,KMnO4和一般浓度的盐酸反应,K2Cr2O7需和较浓的盐酸(>6mol?L-1)反应,MnO2需和浓盐酸(>8mol?L-1)反应.以下结论中,不正确的是 ( )
MnO2+4HCl═MnCl2+Cl2↑+2H2O ;其中,KMnO4和一般浓度的盐酸反应,K2Cr2O7需和较浓的盐酸(>6mol?L-1)反应,MnO2需和浓盐酸(>8mol?L-1)反应.以下结论中,不正确的是 ( )
| A、上述反应既属于氧化还原反应,又属于离子反应 |
| B、生成1molCl2转移电子数均为2NA(NA为阿伏加德罗常数) |
| C、氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 |
| D、盐酸的浓度越大,Cl-的还原性越强 |
下列有关化学用语表示正确的是( )
A、聚丙烯的结构简式: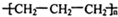 | ||
B、甲醛的电子式: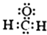 | ||
C、硫原子的结构简式图: | ||
D、中子数为10的氧原子:
|
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、1.8g水中含有中子数为NA |
| B、标准状况下,22.4L CO和C2H4混合气体的总分子数为NA,质量为28g |
| C、1L 0.1mol/L-1稀盐酸中,HCl分子数目为0.1NA |
| D、常温常压下,1mol甲基所含电子数为10NA |