题目内容
9.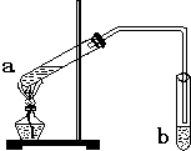 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:(1)a中配置混合溶液时,加入试剂的正确顺序是B(填“A”或“B”);
A.先加入2mL浓硫酸,再慢慢注入2mL乙醇和3mL乙酸
B.先加入2mL乙醇,再慢慢注入2mL浓硫酸和3mL无水乙酸
(2)写出a试管中的主要化学反应的方程式:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O
(3)加入浓H2SO4的目的是催化作用;吸水作用
(4)在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止倒吸.
(5)若要将b试管中的乙酸乙酯分离出来,应采用的实验操作是分液(填操作名称);
(6)将1mol 乙醇(其中的氧用 18O 标记)在浓硫酸存在条件下与足量乙酸充分反应.下列叙述不正确的是B
A.生成的乙酸乙酯中含有18O B.生成的水分子中含有18O
C.可能生成 44g 乙酸乙酯 D.不可能生成 90g 乙酸乙酯.
分析 (1)为防止酸液飞溅,应先加入乙醇,然后在加入浓硫酸和乙酸;
(2)乙酸与乙醇在浓硫酸作用下加热发生酯化反应,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动;
(3)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
(4)球形干燥管除起冷凝作用,同时防止倒吸;
(5)分离互不相溶的液体,可用分液的方法分离;
(6)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应.依据有机酯化反应的本质“酸脱羟基醇脱氢”即可解答.
解答 解:(1)浓硫酸密度比水大,溶于水放出大量的热,为防止酸液飞溅,加入药品时应先在试管中加入一定量的乙醇,然后边加边振荡试管将浓硫酸慢慢加入试管,最后再加入乙酸,
故答案为:B;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(3)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化剂,吸水剂,故答案为:催化作用;吸水作用;
(4)在实验中球形干燥管除起冷凝作用,同时防止倒吸,故答案为:防止倒吸;
(5)分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,故答案为:分液;
(6)将1mol乙醇(其中的氧用18O标记)在浓硫酸存在条件下与足量乙酸充分反应,化学方程式为:CH3COOH+H18OCH2CH3 CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
A.生成的乙酸乙酯中含有18O,故A正确;
B.生成的水分子中不含有18O,故B错误;
C.乙酸乙酯的摩尔质量为88g/mol,1mol乙醇应反应生成1mol乙酸乙酯,但反应是可逆反应,乙酸和乙醇挥发,所以不能进行彻底,应小于90g,可能生成44g乙酸乙酯,故C正确;
D.乙酸乙酯的摩尔质量为88g/mol,1mol乙醇应反应生成1mol乙酸乙酯,但反应不能进行彻底,所以应小于90g,故D正确;
故选B.
点评 本题考查乙酸乙酯的制备,解答时须注意酯化反应的原理和饱和碳酸钠溶液的作用,题目难度不大.

 阅读快车系列答案
阅读快车系列答案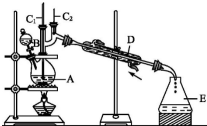 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4},△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4},△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.810 9 | 微溶 |
| 正丁醛 | 75.7 | 0.801 7 | 微溶 |
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸气出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止液体暴沸.若加热后发现未加沸石,应采取的正确方法是冷却后补加.
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)分液漏斗使用前必须进行的操作是C(填正确答案标号).
A.润湿B.干燥 C.检漏 D.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在下层(填“上”或“下”).
(6)反应温度应保持在90~95℃,其原因是为了将正丁醛及时分离出来,促使反应正向进行,并减少正丁醛进一步氧化.
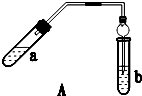 实验室制乙酸乙酯得主要装置如图A所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出纯净的乙酸乙酯.
实验室制乙酸乙酯得主要装置如图A所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出纯净的乙酸乙酯.请回答下列问题:
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑.
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是防止倒吸,步骤⑤中分离乙酸乙酯必须使用的一种仪器是分液漏斗.
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
| 实验 编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是大量乙酸、乙醇未经反应就脱离反应体系;温度过高发生其他反应.
④分离出乙酸乙酯层后,经过洗涤,为了干燥乙酸乙酯可选用的干燥剂为B(填字母).
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体.
| 密度/(g•cm-3) | 沸点/℃ | 水溶性 | |
| 1-丁醇 | 0.81 | 117.7 | 可溶 |
| 乙 酸 | 1.05 | 117.9 | 互溶 |
| 乙酸丁酯 | 0.88 | 126.3 | 微溶 |
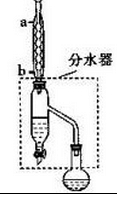
(1)装置a的名称是球形冷凝管,其中冷却水的流动方向是下口进上口出.
(2)制取乙酸丁酯的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.加热回流时,分水器中液体分为两层,适时放出水使上层液体流入烧瓶b,从平衡角度考虑,分水器的作用是除去酯化反应生成的水,使生成乙酸丁酯的平衡向正反应方向移动.
(3)反应结束后,把分水器中的酯层和b中的反应液一起倒入分液漏斗中.在分液漏斗中加入10 mL水洗涤,除去下层,上层继续用10 mL 10% Na2CO3溶液洗涤至中性,分液后将上层液体再用10 mL水洗涤,除去溶于酯中的少量无机盐.下列说法不正确的是D(填序号).
A.最初用10 mL水洗涤的目的是除去酸及少量的正丁醇
B.用10 mL 10% Na2CO3洗涤的目的是除去残留的硫酸和乙酸
C.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口到出
D.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
(4)在洗涤、分液后的乙酸丁酯中加入少量无水硫酸镁,其目的是除去乙酸丁酯中的水(或干燥乙酸丁酯).
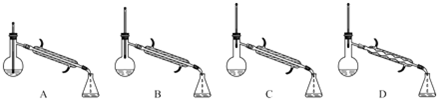
(5)在蒸馏操作中,仪器选择及安装都正确的是C(填标号).
(6)本实验的产率是74%.
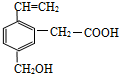 ,关于该有机物的叙述正确的是( )
,关于该有机物的叙述正确的是( )| A. | 不能跟NaOH溶液反应 | |
| B. | 能使溴的四氯化碳溶液褪色,1moL该物质因加成反应消耗溴2mol | |
| C. | 既能与乙酸发生酯化反应,又能与乙醇发生酯化反应 | |
| D. | 在足量的氧气中燃烧1mol该有机物生成H2O 7 mol |
 Fe(SCN)3(血红色) +3KCl,向溶液中加入KCl固体可快速看到血红色
Fe(SCN)3(血红色) +3KCl,向溶液中加入KCl固体可快速看到血红色 2O与NH4Cl的反应是放热反应
2O与NH4Cl的反应是放热反应