题目内容
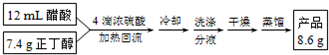
4.乙酸丁酯是优良的有机溶剂,因有愉快的果香气味,也用于香料工业.实验室制取乙酸丁酯的有关信息及装置示意图如下:| 密度/(g•cm-3) | 沸点/℃ | 水溶性 | |
| 1-丁醇 | 0.81 | 117.7 | 可溶 |
| 乙 酸 | 1.05 | 117.9 | 互溶 |
| 乙酸丁酯 | 0.88 | 126.3 | 微溶 |
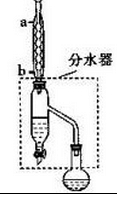
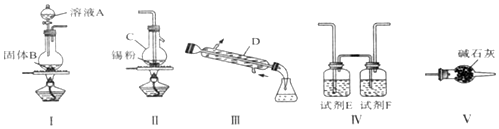
(1)装置a的名称是球形冷凝管,其中冷却水的流动方向是下口进上口出.
(2)制取乙酸丁酯的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.加热回流时,分水器中液体分为两层,适时放出水使上层液体流入烧瓶b,从平衡角度考虑,分水器的作用是除去酯化反应生成的水,使生成乙酸丁酯的平衡向正反应方向移动.
(3)反应结束后,把分水器中的酯层和b中的反应液一起倒入分液漏斗中.在分液漏斗中加入10 mL水洗涤,除去下层,上层继续用10 mL 10% Na2CO3溶液洗涤至中性,分液后将上层液体再用10 mL水洗涤,除去溶于酯中的少量无机盐.下列说法不正确的是D(填序号).
A.最初用10 mL水洗涤的目的是除去酸及少量的正丁醇
B.用10 mL 10% Na2CO3洗涤的目的是除去残留的硫酸和乙酸
C.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口到出
D.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出
(4)在洗涤、分液后的乙酸丁酯中加入少量无水硫酸镁,其目的是除去乙酸丁酯中的水(或干燥乙酸丁酯).
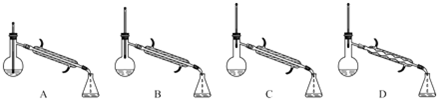
(5)在蒸馏操作中,仪器选择及安装都正确的是C(填标号).
(6)本实验的产率是74%.
分析 由制备实验流程可知,醋酸与正丁醇发生酯化反应生成乙酸丁酯,冷却后加饱和碳酸钠溶液、分液后,干燥、蒸馏得到乙酸丁酯,
(1)a为冷凝管,冷水下进上出;
(2)发生酯化反应生成CH3COOCH2CH2CH2CH3、H2O,分离出水利用平衡正向移动;
(3)碳酸钠溶液可除去酸、醇、降低酯的溶解度,分液时避免上下层液体混合;
(4)无水硫酸镁可吸收水;
(5)温度计测定馏分的温度,温度计的水银球在支管口处,冷水下进上出;
(6)结合CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O计算.
解答 解:(1)装置a的名称是球形冷凝管,其中冷却水的流动方向是下口进上口出,故答案为:球形冷凝管;下口进上口出;
(2)制取乙酸丁酯的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.加热回流时,分水器中液体分为两层,适时放出水使上层液体流入烧瓶b,从平衡角度考虑,分水器的作用是除去酯化反应生成的水,使生成乙酸丁酯的平衡向正反应方向移动,
故答案为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O;除去酯化反应生成的水,使生成乙酸丁酯的平衡向正反应方向移动;
(3)A.最初用10 mL水洗涤的目的是除去酸及少量的正丁醇,与酯分层,故A正确;
B.用10 mL 10% Na2CO3洗涤的目的是除去残留的硫酸和乙酸,与酯分层,故B正确;
C.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从上口到出,可避免上下层液体混合,故C正确;
D.分液时先将水层从分液漏斗的下口放出,再将乙酸丁酯从下口放出,操作不合理,故D错误;
故答案为:D;
(4)在洗涤、分液后的乙酸丁酯中加入少量无水硫酸镁,其目的是除去乙酸丁酯中的水(或干燥乙酸丁酯),
故答案为:除去乙酸丁酯中的水(或干燥乙酸丁酯);
(5)温度计测定馏分的温度,温度计的水银球在支管口处,冷水下进上出,球形干燥管易残留有机物,只有C最合理,
故答案为:C;
(6)CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O
74 116
7.4g x
则x=$\frac{116×7.4g}{74}$=11.6g,
本实验的产率为$\frac{8.6g}{11.6g}$×100%=74%,
故答案为:74%.
点评 本题考查有机物的制备实验,为高频考点,把握有机物的性质、有机反应、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意产率的计算方法,题目难度不大.

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案①C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
②H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H2=-285.8kJ/mol
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H3=-870.3kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
| A. | △H=+244.1kJ/mol | B. | △H=-488.3kJ/mol | C. | △H=-996.6kJ/mol | D. | △H=+996.6kJ/mol |
 H4(g),ΔH=x
H4(g),ΔH=x .x<0,y<0
.x<0,y<0
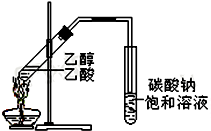 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯.回答下列问题: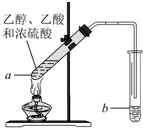 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.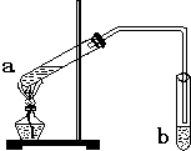 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题: