题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,NA个甲醛分子所占体积约为22.4 L |
| B、电解足量CuCl2溶液时,若电路中转移2NA电子,则阳极一定生成1molCl2 |
| C、同温同压同体积的CO2和SO2所含原子数均为3NA |
| D、0.1 molNa2O2与足量水蒸气反应转移电子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下甲醛为气体,根据标况下气体摩尔体积22.4L/mol计算出甲醛的体积;
B.没有指出电极材料,如果阳极为较活泼的金属电极,则阳极放电的为金属,不会生成氯气;
C.无法计算气体的物质的量,无法计算原子的数目;
D.过氧化钠中氧元素的化合价为-1价,根据反应生成氧气的物质的量计算出转移的电子数.
B.没有指出电极材料,如果阳极为较活泼的金属电极,则阳极放电的为金属,不会生成氯气;
C.无法计算气体的物质的量,无法计算原子的数目;
D.过氧化钠中氧元素的化合价为-1价,根据反应生成氧气的物质的量计算出转移的电子数.
解答:
解:A.NA个甲醛分子的物质的量为1mol,标况下1mol甲醛的体积约为22.4L,故A正确;
B.若电极材料为惰性电极,电路中转移2NA电子,则阳极一定生成1molCl2,而电解材料不是惰性电极时,阳极放电的不是氯离子,则阳极不会生成氯气,故B错误;
C.同温同压同体积的CO2和SO2,含有气体的物质的量相等,但是题中条件无法计算气体的物质的量,所以无法计算含有的原子数,故C错误;
D.0.1mol过氧化钠与足量水反应生成0.05mol氧气,过氧化钠中氧元素化合价为-1价,则生成0.05mol氧气转移了0.1mol电子,转移电子数为0.1NA,故D错误;
故选A.
B.若电极材料为惰性电极,电路中转移2NA电子,则阳极一定生成1molCl2,而电解材料不是惰性电极时,阳极放电的不是氯离子,则阳极不会生成氯气,故B错误;
C.同温同压同体积的CO2和SO2,含有气体的物质的量相等,但是题中条件无法计算气体的物质的量,所以无法计算含有的原子数,故C错误;
D.0.1mol过氧化钠与足量水反应生成0.05mol氧气,过氧化钠中氧元素化合价为-1价,则生成0.05mol氧气转移了0.1mol电子,转移电子数为0.1NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确过氧化钠中氧元素的化合价为-1价,选项B为易错点,注意没有告诉电解材料为惰性电极.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶于少量的浓KOH溶液中:NH4++HCO3-+2OH-═CO32-+NH3↑+2 H2O |
| B、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O |
| C、FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
| D、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
某气态烃1mol恰好与2molHCl加成.生成物分子中的氢又可被6molCl2 取代,则此气态烃可能是( )
| A、CH≡CH |
| B、CH2=CH2 |
| C、CH≡C-CH3 |
| D、CH2=C(CH3)2 |
离子晶体不可能具有的性质是( )
| A、较高的熔、沸点 |
| B、良好的导电性 |
| C、溶于极性溶剂 |
| D、坚硬而易粉碎 |
常温下,下列各组离子或分子在指定溶液中能大量共存的是( )
A、使甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO
| ||||
| B、水电离出的(H+)=1×10-14 mol?L-1的溶液中:Na+、NH4+、Cl-、SiO32- | ||||
| C、c (NaHCO3)=0.1 mol?L-1 的溶液中:K+、C6H5O-、SO42-、CO32- | ||||
D、c(H+)/c(OH-)=1012的溶液中:NH
|
下列有关试剂的保存方法,错误的是( )
| A、铝片直接放置在空气中 |
| B、漂白粉保存在烧杯中 |
| C、新制的氯水通常保存在棕色细口玻璃试剂瓶中 |
| D、氢氧化钠溶液用带橡胶塞的试剂瓶贮存 |
下列装置或操作能达到实验目的是( )
A、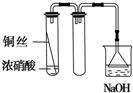 实验室制取NO2 |
B、 证明CO2易溶于水 |
C、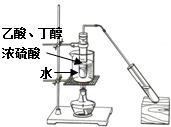 实验室制取乙酸丁酯(沸点126℃) |
D、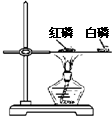 比较红磷与白磷的着火点 |
两种气态烃组成的混合物共0.1mol,完全燃烧后得到4.48LCO2(标准状况下)和3.6g水,则这两种气体可能是( )
| A、CH4和C3H8 |
| B、CH4和C3H4 |
| C、C2H4和C3H4 |
| D、C2H4和C2H6 |