题目内容
【题目】向一定量的NaOH溶液中逐滴加入AlCl3溶液,生成沉淀Al(OH)3的物质的量随AlCl3加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )

A. a点对应的溶液中:Na+、Mg2+、![]() 、
、![]()
B. b点对应的溶液中:Na+、K+、![]() 、Cl-
、Cl-
C. c点对应的溶液中:Ag+、Ca2+、![]() 、Cl-
、Cl-
D. d点对应的溶液中:K+、![]() 、
、![]() 、
、![]()
【答案】B
【解析】
向一定量的NaOH溶液中逐滴加入AlCl3溶液,反应开始阶段(b点之前),发生的反应为4OH-+Al3+=AlO2-+2H2O;OH-反应完全后(b~c段),继续加入AlCl3溶液,发生反应:3 AlO2-+ Al3++6H2O=4Al(OH)3↓;AlO2-反应完全后(c点之后),继续加入 AlCl3溶液,Al(OH)3的物质的量保持不变,结合以上分析解答。
向一定量的NaOH溶液中逐滴加入AlCl3溶液,反应开始阶段(b点之前),发生的反应为4OH-+Al3+=AlO2-+2H2O;OH-反应完全后(b~c段),继续加入AlCl3溶液,发生反应:3 AlO2-+ Al3++6H2O=4Al(OH)3↓;AlO2-反应完全后(c点之后),继续加入 AlCl3溶液,Al(OH)3的物质的量保持不变;
A、向NaOH溶液中逐渐加入AlCl3溶液时发生Al3++4OH-=AlO2-+2H2O,3AlO2-+6H2O+Al3+=4Al(OH)3↓,a点时溶液中有大量OH-,与Mg2+、HCO3-不能大量共存,故A错误;
B、b点时溶质为NaCl和NaAlO2,所有离子可以大量共存,故B正确;
C、c点时溶质为NaCl,与Ag+不能大量共存,故C错误;
D、d点时溶质为NaCl和AlCl3,Al3+和CO32-发生双水解而不能大量共存,故D错误;
综上所述,本题选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】为了探究化学能与热能的转化,某实验小组设计了如图所示的三套实验装置:
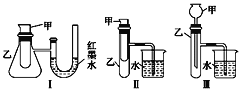
(1)上述3个装置中,不能证明“铜与浓硝 酸反应是吸热反应还是放热反应”的是(不能用手触摸和使用温度计)___________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入 适量氢氧化钠溶液与稀盐酸,U形管中可观察到的现象是______________,说明该反应属于_____ (填“吸热”或“放热”)反应。
(3)为定量测定(2)中反应的反应热,使50 mL 0.50 mol·L-1盐酸与50 mL0.55 mol·L-1NaOH溶液在简易量热计中进行中和反应.回答下列问题:
①该实验中NaOH的浓度大于HCl的浓度的作用是_________________________。
②实验中若改用60 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”)。
(4)已知一些化学键的键能数据如表所示:
化学键 | C—H | C—F | H—F | F—F |
键能/kJ·mol-1 | 414 | 489 | 565 | 155 |
请根据键能数据估算CH4(g)和F2(g)反应生成CF4(g)和HF(g)的热化学方程式:_______________。