题目内容
工业上用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其生产流程如下图所示。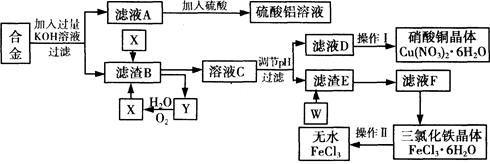
已知:调节适当PH范围可使Fe3+沉淀完全而Cu2+不会沉淀。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式: 。
(2)在滤液A中直接加入硫酸后所得到的硫酸铝溶液中除含少量硫酸外,还一定含有的杂质是
(填化学式)。
请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液,仿照上图形式画出制备流程图(提示:在箭头上下方标出所用试剂和实验操作) 。
(3) 写出试剂X的名称 。
(4) 实验操作I的顺序依次为 (选填序号)。
| A.蒸馏 | B.蒸发浓缩 | C.过滤 | D.冷却结晶 |
(6)写出滤渣E与W反应的化学方程式: 。
(1)2Al+2OH—+2H2O=2AlO2—+3H2↑ (2)K2SO4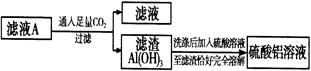 (合理即给分)
(合理即给分)
(3)稀硝酸 (4)BDC (5)重结晶
(6)Fe(OH)3+3HCl=FeCl3+3H2O
解析试题分析: 金属铝可以与氢氧化钾、水反应生成偏铝酸钾和氢气,过量的氢氧化钾会与硫酸反应生成硫酸钾,所以滤液A中肯定还含有硫酸钾,由于偏铝酸根离子在弱酸的条件下可生成沉淀氢氧化铝,所以由滤液A制备纯净的硫酸铝溶液流程为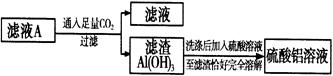 ,稀硝酸能溶解铜和铁,因此X为稀硝酸,。操作I是溶液变成了结晶体,因此操作I的顺序依次为蒸发浓缩、冷却结晶、过滤。要制得更纯的Cu(NO3)2·6H2O晶体,必须进行的操作是重结晶。滤渣E为Fe(OH)3,滤渣E与W反应Fe(OH)3+3HCl=FeCl3+3H2O
,稀硝酸能溶解铜和铁,因此X为稀硝酸,。操作I是溶液变成了结晶体,因此操作I的顺序依次为蒸发浓缩、冷却结晶、过滤。要制得更纯的Cu(NO3)2·6H2O晶体,必须进行的操作是重结晶。滤渣E为Fe(OH)3,滤渣E与W反应Fe(OH)3+3HCl=FeCl3+3H2O
考点:考查化学实验物质制备的相关知识点。

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案通过对金属钠与水反应现象的观察,不能分析得出的结论是( )
| A.金属钠熔点低 | B.金属钠导电性强 |
| C.金属钠密度小 | D.金属钠化学性质活泼[来源 |
碳酸钠(Na2CO3)俗称纯碱,是一种重要的基础化工原料,广泛应用于玻璃、造纸等工业。下列与碳酸钠有关的说法正确的是:
| A.Na2CO3的稳定性介于Na2CO3·10H2O和NaHCO3之间 |
| B.“侯氏制碱法”制得的碱是指NaHCO3 |
| C.可用盐酸鉴别Na2CO3和NaHCO3固体 |
| D.纯碱有时可代替烧碱使用,比如溶解石英、促进乙酸乙酯的水解等 |
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是
| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( )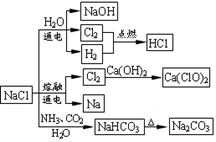
| A.石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| B.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C.常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| D.图中所示转化反应都是氧化还原反应 |
(12分)某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验: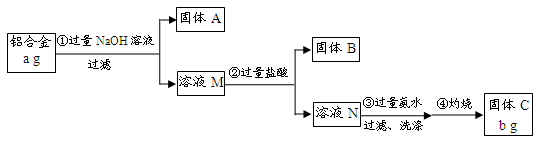
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ;
(2)生成固体B的离子方程式为 ;
步骤③中生成沉淀的离子方程式为 ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为
;
(4)该样品中铝的质量分数是 ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ;
| A.第①步中加入NaOH溶液不足 | B.第②步中加入盐酸不足时 |
| C.第③步中沉淀未用蒸馏水洗涤 | D.第④步对沉淀灼烧不充分 |
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第 周期第 族;W的原子半径比X的
(填“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是 。氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是 ;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
(4)在25℃、101kPa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是 。