题目内容
9.向40mL1mol•L-1的AlCl3溶液中加入100mLKOH溶液,充分反应得到0.78g沉淀,则KOH溶液的物质的量浓度是多少?分析 由Al3++3OH-=Al(OH)3↓和Al(OH)3+OH-=AlO2-+2H2O,可知KOH存在两种情况,一是KOH不足,部分Al3+转化为Al(OH)3,二是Al3+全转化为Al(OH)3后,Al(OH)3部分溶解,以此计算.
解答 解:充分反应得到0.78g沉淀,Al(OH)3的物质的量为$\frac{0.78g}{78g/mol}$=0.01mol,
若KOH不足,由Al3++3OH-=Al(OH)3↓可知n(NaOH)=0.01mol×3=0.03mol,则KOH溶液的物质的量浓度是$\frac{0.03mol}{0.1L}$=0.3mol/L;
若KOH过量,则Al3+全转化为Al(OH)3后,Al(OH)3部分溶解,
Al3++3OH-=Al(OH)3↓
0.04mol 0.12mol 0.04mol
Al(OH)3+OH-=AlO2-+2H2O,
(0.04-0.01)mol 0.03mol
故KOH溶液的物质的量浓度为$\frac{0.12mol+0.03mol}{0.1L}$=1.5mol/L,
答:KOH溶液的物质的量浓度是0.3 mol•L-1或1.5mol•L-1.
点评 本题考查化学反应的计算,为高考常见题型,把握发生的反应及物质的量关系为解答的关键,侧重于学生的分析能力和计算能力的考查,注意氢氧化铝的两性,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
20.下列说法中错误的是( )
| A. | 常温下硫的氧化物都是气体,通入水中都形成强酸 | |
| B. | 将FeCl3滴入饱和H2S溶液中,溶液的pH降低 | |
| C. | 将CO2通入CaSO4溶液中,无明显现象 | |
| D. | 充分利用含硫矿物,既可实现资源的有效利用,还可减轻酸雨污染 |
1.常温下,将铝投入下列物质中,有H2产生的是( )
| A. | 氢氧化钠溶液 | B. | 食盐水 | C. | 浓硫酸 | D. | 盐酸 |
4.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H2=+206.1kJ•mol-1
③焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ•mol-1 .
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H2=+206.1kJ•mol-1
③焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ•mol-1 .
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②使用催化剂,△H2减小 | |
| C. | 反应③中反应物的总能量高于生成物的总能量 | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=+74.8kJ•mol-1 |
14.粗盐的提纯使用的主要仪器有:①漏斗 ②烧杯 ③蒸发皿 ④酒精灯 ⑤量筒 ⑥试管夹 ⑦玻璃棒⑧集气瓶 ⑨天平( )
| A. | ①②③④⑦ | B. | .①②③④⑤ | C. | .①②③⑥⑧ | D. | .③④⑦⑧⑨ |
1.下列离子反应方程式错误的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Ba(OH)2溶液与H2SO4溶液反应:Ba2++2H++2OH-+SO42-═BaSO4↓+2H2O | |
| C. | Na2CO3溶液与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | NH4Cl 溶液显酸性:NH4++H2O?NH3•H2O+H+ |
19.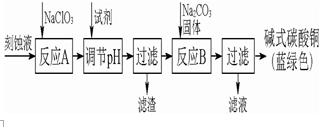 碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:
碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:
(1)氯酸钠的作用是将Fe2+氧化成Fe3+并最终除去;滤渣的主要成分是Fe(OH)3(写化学式).
(2)反应A后调节溶液的pH范围应为3.2-4.2.可以选择的试剂是bd(填序号).
a.氨水 b.氧化铜 c.氧化镁 d.碳酸铜 e..稀氢氧化钠
(3)反应B的温度若过高,则所得蓝绿色产品中可能会出现的杂质是CuO.(写化学式)
(4)洗涤过滤得到的产品时,如何判断产品已经洗净?取最后一次洗涤液,加入硝酸银和稀硝酸,无沉淀生成则表明已洗涤干净.
(5)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀.
①若沉淀只有CuCO3,则相应的离子方程式为Cu2++CO32-=CuCO3↓.
②若沉淀只有Cu(OH)2,用相应的离子方程式表示其过程:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑.
 碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:
碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如图图所示.Cu2+、Fe2+、Fe3+生成沉淀的pH如表格所示:| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
(2)反应A后调节溶液的pH范围应为3.2-4.2.可以选择的试剂是bd(填序号).
a.氨水 b.氧化铜 c.氧化镁 d.碳酸铜 e..稀氢氧化钠
(3)反应B的温度若过高,则所得蓝绿色产品中可能会出现的杂质是CuO.(写化学式)
(4)洗涤过滤得到的产品时,如何判断产品已经洗净?取最后一次洗涤液,加入硝酸银和稀硝酸,无沉淀生成则表明已洗涤干净.
(5)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀.
①若沉淀只有CuCO3,则相应的离子方程式为Cu2++CO32-=CuCO3↓.
②若沉淀只有Cu(OH)2,用相应的离子方程式表示其过程:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑.