题目内容
2.通过火法冶金炼出的铜是粗铜,含有Zn、Fe、Ag、Au等杂质.在实验室条件下用CuSO4溶液作电解液进行电解精炼,并对电解废液进行综合处理.(1)电解精炼铜时粗铜板作阳极,阴极电极反应式为Cu2++2e-═Cu.电解过程中,电解液中c(Cu2+)变小(填变大、变小、不变).对电解废液进行如下处理

已知:①某些金属离子形成氢氧化物沉淀的pH如表
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 4.7 | 5.4 |
| 完全沉淀 | 3.2 | 9.7 | 6.7 | 8.0 |
(2)滤液l中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加NaOH溶液调节溶液pH的范围是3.2≤pH<4.7.
(4)滤渣1跟稀HNO3反应的化学方程式是3Ag+4HNO3═3AgNO3+NO↑+2H2O.
分析 (1)电解精炼铜时,精铜做阴极,粗铜作阳极,阴极上是铜离子得电子;根据锌、铁与硫酸铜发生置换反应分析;
(2)滴加H2O2能将亚铁离子氧化为三价铁离子便于除去,且不引入杂质,据此书写方程式;
(3)慢慢加入氢氧化钠,搅拌,以控制溶液pH,目的是让三价铁离子完全沉淀,铜离子不沉淀;
(4)根据精炼铜原理,滤渣1为比铜还不活泼的Ag、Au,金属银可以和硝酸反应得到硝酸银以及水和一氧化氮,金不反应,据此书写方程式.
解答 解:(1)在电解精炼铜时,阳极反应是金属锌、铁、镍等先失电子,阴极上是铜离子得电子产生铜,电解反应为:Cu2++2e-═Cu,精铜做阴极,粗铜作阳极;硫酸铜的浓度会变小,原因是锌、铁与硫酸铜发生置换反应,故答案为:阳;Cu2++2e-═Cu;变小;
(2)滴加H2O2能将亚铁离子氧化为三价铁离子便于除去,过氧化氢为氧化剂,二价铁为还原剂,所以反应为2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)除去铁离子得到纯净的硫酸铜溶液,根据沉淀PH范围可知,应调节PH,使三价铁完全沉淀,铜离子不沉淀,所以加NaOH溶液调节溶液pH的范围是3.2≤pH<4.7,故答案为:3.2≤pH<4.7;
(4)金属银可以和稀硝酸反应生成硝酸银、一氧化氮和水,金不反应,所以滤渣1与硝酸反应的化学方程式为:3Ag+4HNO3═3AgNO3+NO↑+2H2O;故答案为:3Ag+4HNO3═3AgNO3+NO↑+2H2O.
点评 本题考查了电解精炼铜原理以及电解液的分离与提纯,综合性较强,考查角度广,难度较大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
12.现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第二周期ⅠA族;元素④与元素⑦相比较,气态氢化物较稳定的是NH3(填化学式).
(2)元素①与元素⑥按照原子个数比为1:1形成的化合物中化学键的类型为离子键、共价键.
(3)Y和Z均由元素①组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应.
Ⅰ.Y与Z的关系是(选填字母)b.
a.同位素 b.同素异形体 c.同系物 d.同分异构体
Ⅱ.将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区分二者的实验方法:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2,若溶液不变红,则原通入气体是O3
(4)元素⑤的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量.写出该反应的热化学方程式:Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4Q kJ/mol.
(5)元素①单质和元素⑧单质在海水中可以形成原电池,写出正极反应式:O2+4e-+2H2O═4OH-.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 (10-10m) | 0.73 | 1.02 | 1.34 | 1.06 | 0.99 | 1.54 | 0.75 | 1.18 |
| 最高或最 低化合价 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -2 | -3 | -1 | -3 |
(1)元素③在周期表中的位置是第二周期ⅠA族;元素④与元素⑦相比较,气态氢化物较稳定的是NH3(填化学式).
(2)元素①与元素⑥按照原子个数比为1:1形成的化合物中化学键的类型为离子键、共价键.
(3)Y和Z均由元素①组成,反应Y+2I-+2H+═I2+Z+H2O常作为Y的鉴定反应.
Ⅰ.Y与Z的关系是(选填字母)b.
a.同位素 b.同素异形体 c.同系物 d.同分异构体
Ⅱ.将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区分二者的实验方法:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2,若溶液不变红,则原通入气体是O3
(4)元素⑤的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量.写出该反应的热化学方程式:Cl2O7(l)+H2O(l)═2HClO4(aq)△H=-4Q kJ/mol.
(5)元素①单质和元素⑧单质在海水中可以形成原电池,写出正极反应式:O2+4e-+2H2O═4OH-.
13.下列反应的离子方程式不正确的是( )
| A. | 溴化亚铁溶液中通入过量氯气.2Fe2++2Br-+2C12═2Fe3++Br2+4C1- | |
| B. | 草酸和少量烧碱溶液:H2C2O4+OH-═HC2O4-+H2O | |
| C. | 漂白粉溶液吸收过量的二氧化碳:ClO-十H2O+CO2═HClO+HCO3- | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全NH4++H++SO42-+Ba2++2OH-═NH3•H2O+BaSO4↓+H2O |
17.下列关于0.3mol氧气和0.2mol臭氧气(O3)的说法正确的是( )
| A. | 原子数之比为3:2 | B. | 同温同压下密度比是2:3 | ||
| C. | 同温同压下质量比是3:2 | D. | 标准状况下体积比是2:3 |
7.有关元素X、Y、Z、D、E的信息如下
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是②③(填序号).
①保存EY2溶液时,需向溶液加入少量E单质.
②通常实验室配制EY3溶液时,直接用水溶解EY3固体即可.
③EY2只能通过置换反应生成,EY3只能通过化合反应生成.
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒.
(3)用化学符号表示D2Z的水溶液中各离子浓度从大到小的顺序是Na+>S2->OH->HS->H+.
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm. |
| Y | 所在主族序数与所在周期序数之差为4. |
| Z | 原子半径为0.102nm,核外最外层电子数是其电子层数的2倍,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰. |
| D | 最高价氧化物对应的水化物,能电离出离子数、电子数都相等的阴、阳离子. |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏. |
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法不正确的是②③(填序号).
①保存EY2溶液时,需向溶液加入少量E单质.
②通常实验室配制EY3溶液时,直接用水溶解EY3固体即可.
③EY2只能通过置换反应生成,EY3只能通过化合反应生成.
④铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒.
(3)用化学符号表示D2Z的水溶液中各离子浓度从大到小的顺序是Na+>S2->OH->HS->H+.
14.如表各组关于强电解质、弱电解质、非电解质的归类正确的( )
| A | B | C | D | |
| 强电解质 | C | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | HCl | H2O |
| 非电解质 | 蔗糖 | BaSO4 | C2H5OH | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
11.晶须,是晶体结晶时,形成如胡须状的完美晶体,具有很高的强度.一种直径为1.6μm的铁晶须,抗拉强度可以达到工业纯铁抗拉强度的70倍,而且比经过特殊处理的超高强度的钢的强度还要高出4~10倍.下列分析正确的是( )
| A. | 铁晶须是合金 | B. | 铁晶须不与酸反应 | ||
| C. | 铁晶须可被磁铁吸引 | D. | 铁晶须易溶于水 |
12.甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用如图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).

实验操作和现象:
(1)A中反应的化学方程式是Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)C中白色沉淀是BaSO4(化学式).
(3)C溶液中发生的离子方程式为3SO2+3Ba2++2NO3-+2H2O═3BaSO4↓+2NO↑+4H+.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是通N2一段时间,排除装置中的空气
乙在A、B间增加洗气瓶D,D中盛放的试剂是浓硫酸或饱和NaHSO3溶液.
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸.用离子方程式解释乙产生少量白色沉淀的原因:2Ba2++2SO2+O2+2H2O═2BaSO4↓+4H+.

实验操作和现象:
| 操 作 | 现 象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C 中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中白色沉淀是BaSO4(化学式).
(3)C溶液中发生的离子方程式为3SO2+3Ba2++2NO3-+2H2O═3BaSO4↓+2NO↑+4H+.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是通N2一段时间,排除装置中的空气
乙在A、B间增加洗气瓶D,D中盛放的试剂是浓硫酸或饱和NaHSO3溶液.
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |

 ,
, .写出H→I的反应方程式
.写出H→I的反应方程式 .
. 或
或 .
.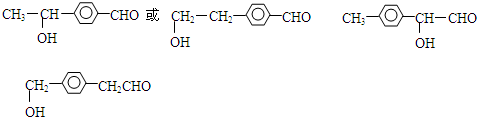 .
.