题目内容
11.充分燃烧一定量丁烷,生成CO2和液态水,放出热量x kJ,将此CO2完全吸收生成正盐,需5mol/L的KOH溶液100ml,则丁烷的燃烧热为( )| A. | 16x kJ•mol-1 | B. | 8x kJ•mol-1 | C. | 4x kJ•mol-1 | D. | 2x kJ•mol-1 |
分析 根据CO2与KOH的反应,计算丁烷燃烧生成的CO2的物质的量,根据C元素守恒计算出丁烷的物质的量,反应放出的热量与丁烷的物质的量成正比,据此计算判断.
解答 解:n(KOH)=0.1L×5mol/L=0.5mol,则由CO2~2KOH可知,n(CO2)=0.5mol×$\frac{1}{2}$=0.25mol,由碳元素守恒则n(C4H10)=$\frac{1}{4}$n(CO2)=$\frac{1}{4}$×0.25mol=$\frac{1}{16}$mol,$\frac{1}{16}$mol丁烷放出的热量为x,所以1mol丁烷完全燃烧放出的热量为16x,则丁烷的燃烧热为16x kJ•mol-1,
故选A.
点评 本题考查反应热的计算,题目难度不大,根据氢氧化钾确定丁烷的物质的量是解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6. 如图表示25℃时,稀释HClO、CH3COOH两种酸的稀溶液时,溶液pH随加水量的变化情况.下列说法不正确的是( )
如图表示25℃时,稀释HClO、CH3COOH两种酸的稀溶液时,溶液pH随加水量的变化情况.下列说法不正确的是( )
 如图表示25℃时,稀释HClO、CH3COOH两种酸的稀溶液时,溶液pH随加水量的变化情况.下列说法不正确的是( )
如图表示25℃时,稀释HClO、CH3COOH两种酸的稀溶液时,溶液pH随加水量的变化情况.下列说法不正确的是( )| A. | 由图可知I为CH3COOH、II为HClO | |
| B. | 图中a、c两点处的溶液中$\frac{c(HR)•c(O{H}^{-})}{c({R}^{-})}$相等(HR代表CH3COOH或HClO) | |
| C. | 图中a点酸溶液浓度大于b点酸溶液浓度 | |
| D. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+) |
2.如图所示的实验操作与方法正确的是( )
| A. | 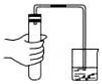 检验装置气密性 | B. | 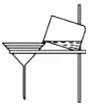 过滤 | C. |  点燃酒精灯 | D. | 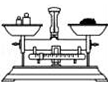 称量氯化钠 |
19.下列说法中正确的是(NA代表阿伏加德罗常数的值)( )
| A. | 28 g N2和28 g CO所含的分子数都是NA | |
| B. | 2 g H2和2g O2所含的原子数都是NA | |
| C. | 28 g CO和44 g CO2所含的氧原子数都是2NA | |
| D. | 98 g H2SO4和98 g H3PO4所含的氧分子数都是4NA |
6.化学与生活密切相关,下列有关说法正确的是( )
| A. | 硅晶体具有半导体性能,可用于制取光导纤维 | |
| B. | 二氧化硫不仅可以漂白纸浆还可用于杀菌消毒 | |
| C. | SO2、NO2或CO2都会导致酸雨的形成 | |
| D. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
16.Fe(OH)3胶体和MgCl2溶液共同具备的性质是( )
| A. | 加热时,二者均能稳定存在 | B. | 两者均有丁达尔效应 | ||
| C. | 加入盐酸先沉淀,后溶解 | D. | 分散质微粒可通过滤纸 |
3.下列分类正确的是( )
| A. |  | |||||||
| B. |  | |||||||
| C. |  | |||||||
| D. |
| |||||||
1. 二氧化硫能起漂白、保鲜作用,使物品颜色显得白亮、鲜艳.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).下列有关说法正确的是( )
二氧化硫能起漂白、保鲜作用,使物品颜色显得白亮、鲜艳.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).下列有关说法正确的是( )
 二氧化硫能起漂白、保鲜作用,使物品颜色显得白亮、鲜艳.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).下列有关说法正确的是( )
二氧化硫能起漂白、保鲜作用,使物品颜色显得白亮、鲜艳.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).下列有关说法正确的是( )| A. | 蓝色石蕊试纸变红后褪色 | |
| B. | NaOH溶液可用于除去实验中多余的SO2 | |
| C. | 湿润淀粉KI试纸未变蓝,说明SO2有还原性 | |
| D. | 品红试纸、蘸有KMnO4溶液的滤纸均褪色,证明了SO2的漂白性 |

 ,D的电子式
,D的电子式 ;
; ;
;