题目内容
以NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A、58.5g氯化钠固体中含有NA个氯化钠分子 |
| B、5.6 g铁粉与酸反应失去的电子数一定为0.2NA |
| C、6.0g金刚石中含有的共价键数为NA |
| D、标况下,11.2LSO3所含的分子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.NaCl为氯化钠的化学式,氯化钠为离子化合物,不存在氯化钠分子;
B.铁与非氧化性酸反应生成亚铁离子,但是与硝酸反应可以生成铁离子;
C.金刚石晶体中,1个C原子与其它4个C形成4个共价键,利用均摊法计算出6g金刚石中含有的共价键数目;
D.标况下三氧化硫的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量.
B.铁与非氧化性酸反应生成亚铁离子,但是与硝酸反应可以生成铁离子;
C.金刚石晶体中,1个C原子与其它4个C形成4个共价键,利用均摊法计算出6g金刚石中含有的共价键数目;
D.标况下三氧化硫的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量.
解答:
解:A.58.5g氯化钠的物质的量为1mol,氯化钠为离子化合物,不存在氯化钠分子,故A错误;
B.5.6g铁的物质的量为0.1mol,0.1mol铁与盐酸、稀硫酸反应失去0.2mol电子,但是与足量稀硝酸反应失去0.3mol电子,故B错误;
C.6g金刚石中含有0.5molC,0.5molC原子可以与其它碳原子形成2mol碳碳共价键,所以1molC形成的共价键为:
×2mol=1mol,含有的共价键数为NA,故C正确;
D.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算11.2L三氧化硫的物质的量,故D错误;
故选C.
B.5.6g铁的物质的量为0.1mol,0.1mol铁与盐酸、稀硫酸反应失去0.2mol电子,但是与足量稀硝酸反应失去0.3mol电子,故B错误;
C.6g金刚石中含有0.5molC,0.5molC原子可以与其它碳原子形成2mol碳碳共价键,所以1molC形成的共价键为:
| 1 |
| 2 |
D.标准状况下,三氧化硫不是气体,不能使用标况下的气体摩尔体积计算11.2L三氧化硫的物质的量,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,选项C为易错点,需要明确金刚石的结构及形成的共价键情况.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列图象分别表示有关反应的反应过程与能量变化的关系 据此判断下列说法正确的是( )
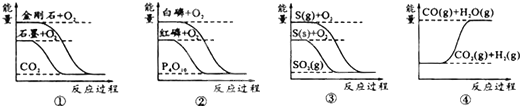

| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、CO (g)+H2O (g)=CO2 (g)+H2 (g)△H<0 |
| D、S (g)+O2 (g)=SO2 (g)△H1; S (s)+O2 (g)=SO2 (g)△H2,则△H1>△H2 |
0.5mol H2含有( )
| A、0.5 mol 个氢气分子 |
| B、6.02×1023个氢气分子 |
| C、3.01×1023个氢气分子 |
| D、3.01×1023个电子 |
某气体的摩尔质量为M g?mol-1,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为x.则
表示的是( )
| Mx |
| VNA |
| A、V L该气体的质量(以g为单位) |
| B、1 L该气体的质量(以g为单位) |
| C、1 mol该气体的体积(以L为单位) |
| D、1 L该气体中所含的分子数 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、lmol FeI2与足量氯气反应时转移的电子数为2NA | ||
B、室温下,14.0g分子通式为CnH2n烯烃中含有的碳碳双键数目为
| ||
| C、标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA | ||
| D、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
下列离子方程式正确的是( )
| A、铝溶于NaOH溶液:Al+2OH-=AlO2-+H2↑ |
| B、过量CO2通入NaOH溶液中:CO2+2OH-=CO32-+H2O |
| C、钠与水反应:2Na+2H2O=2Na++2OHˉ+H2↑ |
| D、稀硫酸中滴加氢氧化钡溶液:H++OH-=H2O |
 如图(图中有部分仪器未画出),有一容积为300ml的注射器,与一500ml的蒸馏烧瓶相连,烧瓶中有0.384g铜片.现向烧瓶中加入18mL2.5mol.L-1的HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口.试回答:
如图(图中有部分仪器未画出),有一容积为300ml的注射器,与一500ml的蒸馏烧瓶相连,烧瓶中有0.384g铜片.现向烧瓶中加入18mL2.5mol.L-1的HNO3溶液,并立即用锡箔包住的橡皮塞封住瓶口.试回答: