题目内容
7.写出下列物质在水溶液中的电离方程式.(1)NaHCO3:NaHCO3═Na++HCO3-.
(2)KAl(SO4)2:KAl(SO4)2=K++Al3++2SO42-.
分析 (1)碳酸氢钠在水中电离出钠离子和碳酸氢根离子;
(2)KAl(SO4)2在水中电离出钾离子、铝离子和硫酸根离子.
解答 解:(1)碳酸氢钠在水中电离出钠离子和碳酸氢根离子,电离方程式为NaHCO3═Na++HCO3-;
故答案为:NaHCO3═Na++HCO3-;
(2)KAl(SO4)2在水中电离出钾离子、铝离子和硫酸根离子,电离方程式为KAl(SO4)2=K++Al3++2SO42-;
故答案为:KAl(SO4)2=K++Al3++2SO42-.
点评 本题考查电离方程式的书写,注意原子团的书写及电离方程式应遵循电荷守恒、质量守恒定律,题目难度不大.

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
17. 工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
(1)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).
500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
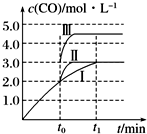
(2)在3L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积(快速)压缩至2 L.
 工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
工业上可用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应 | 平衡 常数 | 温度/℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(2)在3L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ.当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂.当曲线Ⅰ变为曲线Ⅲ时,改变的条件是将容器的体积(快速)压缩至2 L.
18.反应速率v和反应物浓度的关系是用实验的方法测定的,化学反应H2+Cl2═2HCl 的反应速率v可表示为v=k[H2]m[Cl2]n,式中k为常数,m、n值可用表中数据确定.由此可推得,m、n值正确的是( )
| c(H2)/mol•L-1 | c(Cl2)/mol•L-1 | v/(mol•L-1•s-1) |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A. | m=1,n=1 | B. | m=$\frac{1}{2}$,n=$\frac{1}{2}$ | C. | m=$\frac{1}{2}$,n=1 | D. | m=1,n=$\frac{1}{2}$ |
12.有一种有机物A具有抗癌作用,其结构简式为: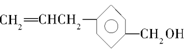 ,下列关于有机物A的说法错误的是( )
,下列关于有机物A的说法错误的是( )
 ,下列关于有机物A的说法错误的是( )
,下列关于有机物A的说法错误的是( )| A. | 有机物A可以与氯气反应 | |
| B. | 有机物A与 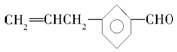 互为同分异构体 互为同分异构体 | |
| C. | 有机物A可与CH3COOH发生酯化反应 | |
| D. | 有机物A可以使酸性KMnO4溶液褪色 |
19.将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个反应:
SO2+2Fe3++2H2O═SO42-+4H++2Fe2+,
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
下列说法正确的是( )
SO2+2Fe3++2H2O═SO42-+4H++2Fe2+,
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
下列说法正确的是( )
| A. | Cr2O72-不能将SO2氧化 | B. | 还原性:Cr3+>Fe2+>SO2 | ||
| C. | 氧化性:Cr2O72->Fe3+>SO2 | D. | 两个反应中Fe3+均表现还原性 |
16.下列物质的主要成分属于硅酸盐的是( )
| A. | 石灰石 | B. | 石英 | C. | 纯碱 | D. | 陶瓷 |

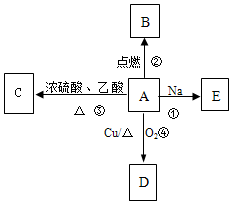 A是易溶于水的有机物C2H5OH,能发生如图所示的多种反应(部分产物已略),D的相对分子质量为44,分子式为C2H4O.请回答下列问题:
A是易溶于水的有机物C2H5OH,能发生如图所示的多种反应(部分产物已略),D的相对分子质量为44,分子式为C2H4O.请回答下列问题: