题目内容
1.化学与人类生产、生活,社会可持续发展密切相关.下列说法正确的是( )| A. | 蔬菜表面洒少许福尔马林,可保鲜和消毒 | |
| B. | 推广使用可降解塑料及布质购物袋,以减少“白色污染” | |
| C. | 绿色食品就是不使用化肥农药,不含任何化学物质的食品 | |
| D. | 推广使用煤液化技术可减少二氧化碳温室气体的排放 |
分析 A.HClO的水溶液为福尔马林,HClO有毒;
B.塑料不能降解,导致白色污染;
C.绿色食品是指在无污染的条件下种植、养殖、施有机肥料、不用高毒性、高残留农药、在标准环境、生产技术、卫生标准下加工生产、经权威机构认定并使用专门标志的安全、优质、营养类食品的统称;
D.煤液化转化为甲醇,减少污染物的排放,提高能源利用率.
解答 解:A.HClO的水溶液为福尔马林,HClO有毒,则不能对蔬菜保鲜和消毒,故A错误;
B.塑料不能降解,导致白色污染,则推广使用可降解塑料及布质购物袋,以减少“白色污染”,故B正确;
C.绿色食品是指在无污染的条件下种植、养殖、施有机肥料、不用高毒性、高残留农药、在标准环境的食品,生产时可以使用有机化肥和低毒的农药,故C错误;
D.煤液化转化为甲醇,减少污染物的排放,提高能源利用率,则推广使用煤液化技术可减少二氧化硫及固体颗粒污染物排放,不能减少二氧化碳气体排放,故D错误;
故选B.
点评 本题考查环境保护及绿色化学,为高频考点,把握物质的性质、化学与生活的联系、环境保护等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
12.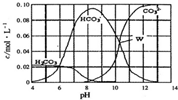 25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
 25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )| A. | W点所示的溶液中:c(Na+)+c(H+)=4c(CO32-)+c(OH-)+c(Cl-) | |
| B. | pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol/L | |
| C. | pH=8的溶液中:c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-) | |
| D. | pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3) |
16.下列说法不正确的是( )
| A. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即盖上盖板,用环形玻璃搅拌棒不断搅拌,准确读出反应体系的最高温度 | |
| B. | 实验事实证明乙酸乙酯中少量乙醇可以用水洗方法除去,其原理与溴水中加四氯化碳萃取溴类似 | |
| C. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度,加快油脂皂化反应速率 | |
| D. | 当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
13.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | 在0.1mol/LNaHCO3 溶液中有:c(Na+)>c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | 在NaHSO4溶液中有:c(Na+)=c(SO42-)=c(H+) | |
| C. | 在新制氯水中加入KOH至溶液呈中性,则溶液中有:c(K+)=2c(ClO-)+C(HClO) | |
| D. | 将等物质的量浓度的Na2SO3溶液和NaHSO4溶液等体积混合后的混合溶液中:c(OH-)-c(H2SO3)=c(H+)+c(SO32-) |
10.铝土矿为自然界中铝的重要存在形式,通常含有50%左右的Al2O3,以及SiO2、Fe2O3和MgO等成分.上述4种氧化物中,属于两性氧化物的是( )
| A. | Al2O3 | B. | SiO2 | C. | Fe2O3 | D. | MgO |
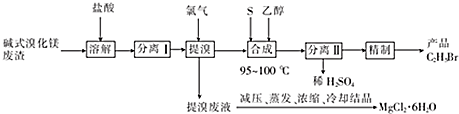
5.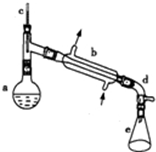 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:
a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.反应粗产物倒入f中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯.
回答下列问题:
(1)由环己醇制取环己烯的方程式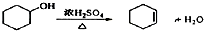 ;
;
(2)装置b的冷凝水方向是下进上出(填下进上出或上进下出);
(3)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验中最容易产生的副产物所含的官能团名称为醚键.
(5)在分离提纯中,使用到的仪器f名称是分液漏斗,分离氯化钙的操作是过滤.
(6)合成过程中加入浓硫酸的作用是催化剂、脱水剂.
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环乙醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
回答下列问题:
(1)由环己醇制取环己烯的方程式
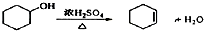 ;
;(2)装置b的冷凝水方向是下进上出(填下进上出或上进下出);
(3)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验中最容易产生的副产物所含的官能团名称为醚键.
(5)在分离提纯中,使用到的仪器f名称是分液漏斗,分离氯化钙的操作是过滤.
(6)合成过程中加入浓硫酸的作用是催化剂、脱水剂.
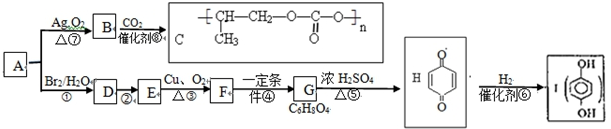
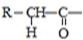 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$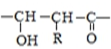
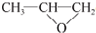 ;⑤的反应类型是消去反应.
;⑤的反应类型是消去反应.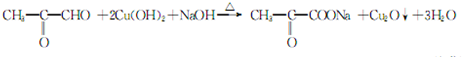 ;
;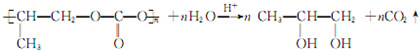 .
.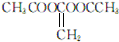 或
或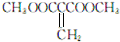 )(任写两种)
)(任写两种)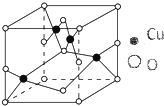 纯铜在工业上主要用来制造导线、电器元件等,铜能形成多种-1和+2价态的化合物且其化合物常带有颜色.
纯铜在工业上主要用来制造导线、电器元件等,铜能形成多种-1和+2价态的化合物且其化合物常带有颜色.