题目内容
1.有NaCl和KCl的混合物25g,溶与水形成溶液,加入1000g 7.14%的AgNO3溶液,充分反应后滤出沉淀,再向混合物加入100g Cu片,过一段时间取出(反应完全),洗涤干燥称其质量为101.52g,求原混合物中NaCl和KCl的物质的量各为多少?分析 向混合物加入100g Cu片,过一段时间取出(反应完全),洗涤干燥称其质量为101.52g,说明加入AgNO3溶液过量,NaCl和KCl反应完全,根据氯守恒和质量守恒联列方程组进行解答.
解答 解:设与Cu反应的硝酸银的物质的量为xCu~~~2AgNO3~~~2Ag△m
64 2mol 2×108 152
xmol 1.52g
则:$\frac{2mol}{xmol}=\frac{152g}{1.52g}$,解得:x=0.02mol
n(AgNO3)=$\frac{1000g×7.14%}{170g/mol}$=0.42mol
由氯守恒得:n(NaCl)+n(KCl)=0.42mol-0.02mol=0.4mol,
根据质量守恒得:n(NaCl)×58.5+n(KCl)×74.5=25,解之得
n(NaCl)=0.3mol n(KCl)=0.1mol,
答:原混合物中NaCl和KCl的物质的量分别为:0.3 mol和0.1 mol.
点评 本题考查混合物的有关计算,侧重考查学生分析计算能力,明确固体质量增加量含义是解本题关键,利用差量法分析解答,题目难度不大.

练习册系列答案
相关题目
16.微波炉加热时,电炉内的微波场以极高的频率改变电场的方向,使水分子迅速摆动而产生热效应.在高频改变方向的电场中水分子会迅速摆动的原因是( )
| A. | 水分子具有极性共价键 | B. | 水分子中有共用电子对 | ||
| C. | 水由氢、氧两种元素的原子组成 | D. | 水分子是极性分子 |
9.用下列装置进行相应实验,能达到实验目的是( )
| A. |  配制一定浓度的稀硫酸 | B. |  实验室制取氨气 | ||
| C. |  蒸发饱和食盐水 | D. | 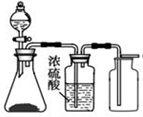 制取、收集氢气 |
16.下列说法中不正确的是( )
| A. | 维勒用无机物合成了尿素,突破了无机物与有机物的界限 | |
| B. | 分子式为C4H8的有机物可能存在4个C-C单键 | |
| C. | (CH3)3CCH2CH(C2H5)CH3 可命名为2,2-二甲基-4-乙基戊烷,核磁共振氢谱有6组峰 | |
| D. | 尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质 |
6.用Cu和HNO3反应制Cu(NO3)2,应选用的方法是( )
| A. | Cu和浓HNO3反应 | B. | Cu和稀HNO3反应 | ||
| C. | 先把Cu粉氧化,再用稀HNO3溶解CuO | D. | 上述任何方法都一样 |
13.下列实验装置或操作正确的是( )
| A. |  从碘水中分离出碘 | B. |  检验试液中NH${\;}_{4}^{+}$的存在 | ||
| C. |  干燥SO2气体 | D. |  收集HCl气体 |
11.如图所示的装置,C.D.E.F.X.Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )
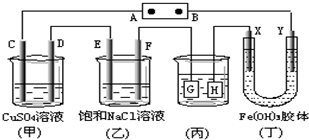

| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |


