题目内容
16.下列关于元素周期表的说法正确的是( )| A. | ⅠA族元素也称为碱金属元素 | |
| B. | 稀有气体元素原子的最外层电子数均为8 | |
| C. | 过渡元素全部是金属元素,因此它们又被称为过渡金属 | |
| D. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
分析 A.IA族包含碱金属与氢元素;
B.氦原子核外只有2个电子;
C.过渡元素全部是金属元素;
D.俄国化学家门捷列夫为元素周期表的建立作出了巨大贡献.
解答 解:A.IA族包含碱金属与氢元素,除氢之外的其它元素属于碱金属,故A错误;
B.氦原子核外只有2个电子,其它稀有气体原子最外层电子数为8,故B错误;
C.过渡元素全部是金属元素,故C正确;
D.俄国化学家门捷列夫为元素周期表的建立作出了巨大贡献,门捷列夫制作出了第一张元素周期表,故D错误;
故选C.
点评 本题考查元素周期表与元素的性质知识,题目较为简单,注意基础知识的积累.

练习册系列答案
相关题目
6.有分子式为C10H20O2的酯A,在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有( )
| A. | 4种 | B. | 8种 | C. | 16种 | D. | 40种 |
7.为了探究影响化学反应速率的因素,4位同学分别设计了下列4个实验,其中结论不正确的是( )
| A. | 将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同 | |
| B. | 盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快 | |
| C. | 将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快 | |
| D. | 升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
11.下列离子方程式书写不正确的是( )
| A. | 氯水和碘化钾反应:Cl2+2I-=2Cl-+I2 | |
| B. | 盐酸与AgNO3溶液反应:HCl+Ag+=H++Ag Cl↓ | |
| C. | 氢氧化钙溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O | |
| D. | 二氧化锰和盐酸制氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
1.如图是某有机物核磁共振氢谱图,但该物质可能是( )
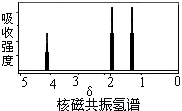

| A. | CH3COOCH2CH3 | B. | CH3CH=CHCH3 | C. | CH3CH2CH3 | D. | CH3CHOHCH3 |
8.液态锂离子电池是指Li+嵌入化合物为正负电极的二次电池.正极采用锂化合物LiCoO2,负极采用碳电极,充电后成为锂-碳层间化合物LixC6(0<x≤1),电解质为溶解有锂盐LiPF6、LiAsF6等的有机溶液.下列有关说法不正确的是( )
| A. | 将LiCoO2改写成为氧化物的形式为Li2O•Co2O3 | |
| B. | 该电池的电解液必须使用有机溶剂主要是由于有机溶剂有良好的导电性 | |
| C. | Li是3号元素,是最轻的金属之一,这类电池质能比高 | |
| D. | 在电池充放电时,Li+在两个电极之间往返嵌入和脱嵌.该电池的充放电反应方程式为:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6 |
10.已知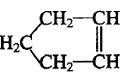 可简写为
可简写为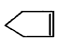 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: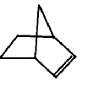
则降冰片烯不具有的性质( )
 可简写为
可简写为 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为:
则降冰片烯不具有的性质( )
| A. | 易溶于水 | B. | 能发生氧化反应 | C. | 能发生加成反应 | D. | 能发生取代反应 |
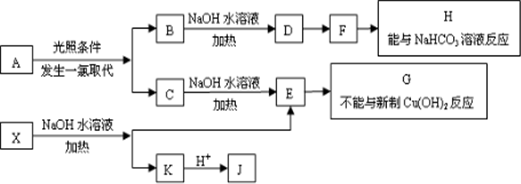
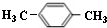 .
.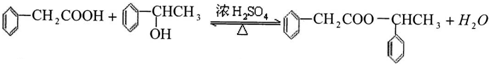 ;该反应类型是酯化反应(或取代反应).
;该反应类型是酯化反应(或取代反应).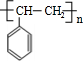 .
.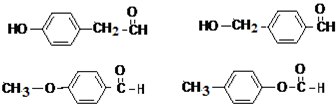 任意一种.
任意一种.