题目内容
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | KAlO2 | 稀硫酸 |
| ② | KOH溶液 | NaHCO3 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
| A、①③ | B、①④ | C、②④ | D、②③ |
考点:镁、铝的重要化合物,钠的重要化合物,铜金属及其重要化合物的主要性质
专题:几种重要的金属及其化合物
分析:①偏铝酸钾只能与酸反应,不能与碱反应;
②NaHCO3是多元弱酸的氢盐,既可以与强酸反应又可以与强碱反应;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应;
④Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁.
②NaHCO3是多元弱酸的氢盐,既可以与强酸反应又可以与强碱反应;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应;
④Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁.
解答:
解:①偏铝酸钾只能与酸反应生成氢氧化铝,不能与碱反应,故①不符合;
②NaHCO3是多元弱酸的氢盐,既可以与盐酸反应生成氯化钠,水和二氧化碳,又可以与氢氧化钾反应生成碳酸盐和水,故②符合;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应,常温下氮气不能与氧气、氢气发生反应,故③不符合;
④常温下,Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁,故④符合,
故选C.
②NaHCO3是多元弱酸的氢盐,既可以与盐酸反应生成氯化钠,水和二氧化碳,又可以与氢氧化钾反应生成碳酸盐和水,故②符合;
③氮气与氧气在放电条件下反应得到NO,氮气与氢气在高温高压、催化剂条件下合成氨气反应,常温下氮气不能与氧气、氢气发生反应,故③不符合;
④常温下,Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,与氯化铁溶液反应得到氯化铜、氯化亚铁,故④符合,
故选C.
点评:本题考查元素化合物性质,难度不大,侧重对基础知识的巩固,需要学生熟练掌握元素化合物性质.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
在进行中和热的测定中,下列操作或说法错误的是( )
| A、不可将温度计当搅拌棒使用,也不可靠在容器内壁上 |
| B、搅拌时,环形玻璃搅拌棒应上下移动 |
| C、测量反应混合液的温度时要随时读取温度,记录下最高温度 |
| D、为了使反应完全,必须保证酸和碱恰好完全反应 |
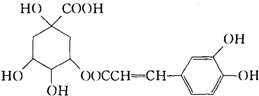 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )| A、2 molNaOH |
| B、4 molNaOH |
| C、6 molNaOH |
| D、8 molNaOH |
现有CuO和Fe2O3组成的混合物a g,向其中加入2mol?L-1的硫酸溶液50mL,恰好完全反应.若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量为( )
| A、1.6a g |
| B、(a-1.6)g |
| C、(a-3.2)g |
| D、1.6 g |
下列各组物质能在同一溶液中大量共存的是( )
| A、CuSO4、H2SO4、HNO3 |
| B、Na2SO4、Ba(OH)2、CuCl2 |
| C、FeCl3、NaOH、KNO3 |
| D、K2SO4、NaOH、NaCl |
下列说法正确的是( )
| A、常温下0.1 mol/L的下列溶液①NH4Al(SO4)2②NH3?H2O③NH4Cl ④CH3COONH4中,c(NH4+)由大到小的顺序是:①>③>④>② |
| B、常温时,pH=2的CH3COOH溶液和pH=12的氨水等体积混合;pH=2的HCl溶液和pH=12的NaOH溶液等体积混合,各混合溶液中由水电离的c(H+)一定相等 |
| C、常温下0.4mol/L HB溶液和0.2mol/L NaOH溶液等体积混合后,则混合后溶液中离子浓度的大小顺序一定为:c(B-)>c(Na+)>c(H+)>c(OH-) |
| D、0.lmol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)>c(OH-) |
金属的腐蚀造成了相当大的经济损失和环境污染,因此,人们想了很多方法防止金属的腐蚀.下面关于金属腐蚀的叙述正确的是( )
| A、铁壳轮船在河水中航行比在海水中航行更易被腐蚀 |
| B、常温下,铁易被干燥的氯气腐蚀 |
| C、钢铁发生吸氧腐蚀时,发生的负极反应为02+4e-+2H20═40H- |
| D、为了防止枪炮表面的钢铁被腐蚀,可以在钢铁表面进行烤蓝处理 |
乙醇催化氧化为乙醛过程中化学键的断裂与形成情况可表示如下:下列醇能被氧化为醛类化合物的是( )

| A、(CH3)3COH |
B、 |
C、 |
| D、CH3CH2CH(CH3)OH. |