题目内容
9.下列各示意图与对应表述正确的是( )| A. |  为证明非金属性强弱:S>C>Si | |
| B. | 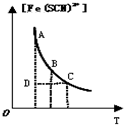 表示可逆反应Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)平衡时,物质的量浓度[Fe(SCN)2+]与温度T的关系,反应处于D点时,一定有V(正)<V(逆) | |
| C. | 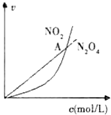 表示恒温恒容条件下发生的可逆反应2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| D. | 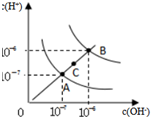 为水的电离平衡曲线图,若从A点到C点,可在水中加入适量NaOH固体 |
分析 A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
B.D在曲线下方,不是平衡状态,c[Fe(SCN)2+]比平衡状态小,应向正反应方向移动;
C.可逆反应2NO2?N204(g)中,分析判断 二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1,说明反应达到平衡状态;
D.C点离子积常数大于A,则C点温度高于A,加入NaOH固体不能实现从A点到C点.
解答 解:A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,硫酸和碳酸钠反应生成碳酸、碳酸和硅酸钠反应生成硅酸,所以能说明非金属性S>C>Si,故A正确;
B.D在曲线下方,不是平衡状态,c[Fe(SCN)2+]比平衡状态小,应向正反应方向移动,V正>V逆,故B错误;
C.可逆反应2NO2?N204(g)中,分析判断,二氧化氮消耗速率和四氧化二氮的消耗速率之比为2:1时才能说明反应达到平衡状态,交点只是浓度相同不能证明达到终点,故C错误;
D.C点离子积常数大于A,则C点温度高于A,加入NaOH固体,溶液中氢氧根离子浓度增大、氢离子浓度减小,不符合图象,所以不能实现从A点到C点,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及非金属性强弱判断、化学平衡状态判断等知识点,侧重考查学生图象分析及判断能力,明确图中曲线变化趋势及变化原理是解本题关键,易错选项是D.

练习册系列答案
相关题目
19.下列实验现象,解释或结论正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中龠Na+,不含K+ |
| B | 向某溶液中滴加KSCN溶液,无明显现象,再滴加 少量氯水,溶液变成红色 | 溶液中含有Fe2+,没有Fe3+ |
| C | 向苯中滴入少量浓溴水,振荡,精置分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 在少量无水乙醇中加入金属Na+,缓慢生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
20.化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A. | 聚乙烯食品袋耐高温加热 | |
| B. | 石英玻璃仪器耐酸碱腐蚀 | |
| C. | 羊毛织物可用强碱性洗涤剂清洗 | |
| D. | 把铅加入锡中制造焊锡的目的是降低熔点 |
17.含氮的化合物广泛存在于自然界,是一类非常重要的化合物.回答下列有关问题:
(1)在一定条件下:2N2(g)+6H2O(g)=4NH3(g)+3O2(g).已知该反应的相关的化学键键能数据如下:
则该反应的△H=+1268kJ/mol.
(2)电厂烟气脱氮的主要反应
I:4NH3(g)+6NO(g)═5N2(g)+6H2O(g)△H<0,副反应
II:2NH3(g)+8NO(g)═5N2O(g)+3H2O(g)△H>0.
①反应I的化学平衡常数的表达式为K=$\frac{{c}^{6}({H}_{2}O){c}^{5}({N}_{2})}{{c}^{6}(NO){c}^{4}(N{H}_{3})}$.
②对于在2L密闭容器中进行的反应I,在一定条件下n(NH3) 和n(N2) 随时间变化的关系如图1所示:
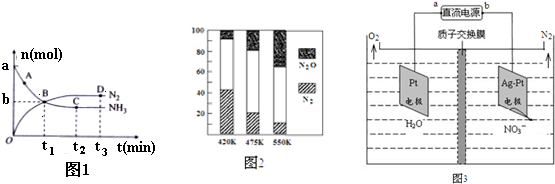
用NH3表示从开始到t1时刻的化学反应速率为$\frac{a-b}{2{t}_{1}}$ (用a、b、t表示)mol/(L•min),图中表示已达平衡的点为CD.
③电厂烟气脱氮的平衡体系的混合气体中N2和N2O含量与温度的关系如图2所示,在温度420~550K时,平衡混合气体中N2O含量随温度的变化规律是随温度升高,N2的含量降低,造成这种变化规律的原因是主反应为放热反应,升温使主反应的平衡左移或者副反应为吸热反应,升温使副反应的平衡右移,降低了NH3和NO浓度,使主反应的平衡左移.
(3)电化学降解法可治理水中硝酸盐的污染.电化学降解NO3-的原理如图3所示,电源正极为a(填“a”或“b”),阴极电极反应式为2NO3-+10e-+12H+=N2+6H2O.
(1)在一定条件下:2N2(g)+6H2O(g)=4NH3(g)+3O2(g).已知该反应的相关的化学键键能数据如下:
| 化学键 | N≡N | H-O | N-H | O=O |
| E/(kJ/mol) | 946 | 463 | 391 | 496 |
(2)电厂烟气脱氮的主要反应
I:4NH3(g)+6NO(g)═5N2(g)+6H2O(g)△H<0,副反应
II:2NH3(g)+8NO(g)═5N2O(g)+3H2O(g)△H>0.
①反应I的化学平衡常数的表达式为K=$\frac{{c}^{6}({H}_{2}O){c}^{5}({N}_{2})}{{c}^{6}(NO){c}^{4}(N{H}_{3})}$.
②对于在2L密闭容器中进行的反应I,在一定条件下n(NH3) 和n(N2) 随时间变化的关系如图1所示:

用NH3表示从开始到t1时刻的化学反应速率为$\frac{a-b}{2{t}_{1}}$ (用a、b、t表示)mol/(L•min),图中表示已达平衡的点为CD.
③电厂烟气脱氮的平衡体系的混合气体中N2和N2O含量与温度的关系如图2所示,在温度420~550K时,平衡混合气体中N2O含量随温度的变化规律是随温度升高,N2的含量降低,造成这种变化规律的原因是主反应为放热反应,升温使主反应的平衡左移或者副反应为吸热反应,升温使副反应的平衡右移,降低了NH3和NO浓度,使主反应的平衡左移.
(3)电化学降解法可治理水中硝酸盐的污染.电化学降解NO3-的原理如图3所示,电源正极为a(填“a”或“b”),阴极电极反应式为2NO3-+10e-+12H+=N2+6H2O.
14.在1.0L密闭容器中放入0.10molA(g),在一定温度进行如下反应:
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
回答下列问题:
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.
A(g)?2B(g)+C(g)+D(s)△H=+85.1kJ•mol-1
容器内气体总压强(P)与起始压强P0的比值随反应时间(t)数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
| $\frac{P}{{P}_{0}}$ | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
(1)下列操作能提高A转化率的是AD
A.升高温度 B.体系中通入A气体
C.通入稀有气体He,使体系压强增大到原来的5倍
D.若体系中的C为HCl,其它物质均难溶于水,滴入少许水
(2)该反应的平衡常数的表达式K=$\frac{{c}^{2}(B)×c(C)}{c(A)}$,前2小时C的反应速率是0.02 mol•L-1•h-1
(3)平衡时A的转化率为70%.
 $\stackrel{HIO_{4}}{→}$
$\stackrel{HIO_{4}}{→}$  +
+
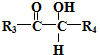 $\stackrel{HIO_{4}}{→}$R3COOH+
$\stackrel{HIO_{4}}{→}$R3COOH+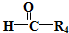
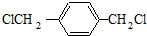 .
.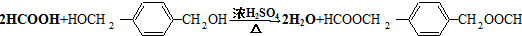 .
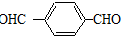
.
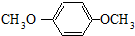

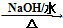 HOCH2CH2OH $\stackrel{HIO_{4}}{→}$HCHO
HOCH2CH2OH $\stackrel{HIO_{4}}{→}$HCHO 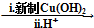 HCOOH
HCOOH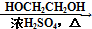 HCOOCH2CH2OOCH.
HCOOCH2CH2OOCH.