题目内容
在配制一定物质的量浓度的硫酸溶液时,下列错误操作可使所配制溶液浓度偏高的是( )
| A、浓硫酸稀释后马上转移至容量瓶 |
| B、溶解搅拌时有液体飞溅 |
| C、容量瓶洗净后没有干燥 |
| D、定容时仰视容量瓶瓶颈刻度线 |
考点:配制一定物质的量浓度的溶液
专题:
分析:分析操作对溶质的物质的量和溶液体积的影响,依据C=
进行误差分析.
| n |
| V |
解答:
解:A.浓硫酸稀释后马上转移至容量瓶,冷却后溶液的体积偏小,溶液的浓度偏高,故A正确;
B.溶解搅拌时有液体飞溅,导致溶质损耗,溶质的物质的量偏小,溶液的浓度偏低,故B错误;
C.容量瓶洗净后没有干燥,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故C错误;
D.定容时仰视容量瓶瓶颈刻度线,导致溶液的体积偏大,溶液的浓度偏低,故D错误;
故选:A.
B.溶解搅拌时有液体飞溅,导致溶质损耗,溶质的物质的量偏小,溶液的浓度偏低,故B错误;
C.容量瓶洗净后没有干燥,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故C错误;
D.定容时仰视容量瓶瓶颈刻度线,导致溶液的体积偏大,溶液的浓度偏低,故D错误;
故选:A.
点评:本题考查了配制一定物质的量浓度溶液实验的误差分析,清楚配制溶液的原理、准确判断不当操作对溶质的物质的量和溶液体积的影响是解题关键.

练习册系列答案
相关题目
下列离子方程式表达正确的是( )
| A、铁粉加入到FeCl3溶液中:Fe+Fe3+=2Fe2+ |
| B、过量的氨水滴加到氯化铝溶液:Al3++4OH-═AlO2-+2H2O |
| C、氯气与水反应:Cl2+H2O═Cl-+2H++ClO- |
| D、硅酸钠溶液中通入过量CO2:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3- |
以下实验装置一般不用于分离物质的是( )
A、 |
B、 |
C、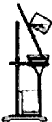 |
D、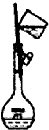 |
将铁、铝的混合物加入到足量氢氧化钠溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的硫酸铜溶液中,充分反应后过滤得到的固体质量正好与原固体质量相等,则原固体中铝的质量分数为( )
| A、14.3% | B、12.5% |
| C、87.5% | D、无法计算 |
下列说法不正确的是( )
| A、用茚三酮溶液可以鉴别甘氨酸与醋酸 |
| B、中和滴定实验中,用于盛放待测液的锥形瓶洗净后未干燥不会影响测定结果 |
| C、现代仪器分析中,常用质谱仪、元素分析仪、红外光谱仪等测定有机物结构,用原子吸收光谱确定物质中含有哪些非金属元素 |
| D、如果不慎将苯酚沾到皮肤上,应立即用酒精洗涤,再用水冲洗 |