题目内容
9.下列叙述正确的是( )| A. | NaOH可用于治疗胃酸过多 | |
| B. | CaO可防止月饼等食品氧化变质 | |
| C. | 氢弹中用到的2H、3H互为同位素 | |
| D. | 向海水中加入净水剂明矾可以使海水淡化 |
分析 A、氢氧化钠是强碱;
B、CaO没有强还原性;
C、同种元素的不同种原子互称同位素;
D、明矾水解出的氢氧化铝能吸附水中的杂质.
解答 解:A、氢氧化钠是强碱,具有强腐蚀性,不能用于胃酸过多的治疗,故A错误;
B、CaO没有强还原性,故不能防止食品的氧化变质,只能起到防潮的作用,故B错误;
C、同种元素的不同种原子互称同位素,故2H、3H互为同位素,故C正确;
D、明矾水解出的氢氧化铝能吸附水中的杂质,不能除去可溶于水的溶质,即不能用于海水的淡化,故D错误.
故选C.
点评 本题考查了化学物质在生产、生活中的应用,注意基础知识和生活经验的积累尤为重要.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
20.下列排列顺序错误的是( )
| A. | 原子半径:O<S<Na | B. | 热稳定性:NH3<PH3<H2S | ||
| C. | 酸性:H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3<Mg(OH)2<NaOH |
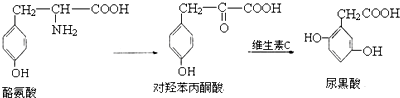
4.尿黑酸症是由酪氨酸在人体内非正常代谢而产生的一种疾病.其转化过程如下:
下列说法错误的是( )

下列说法错误的是( )
| A. | 1mol酪氨酸能与含1molHCl的盐酸反应,又能与含2molNaOH的溶液反应 | |
| B. | 酪氨酸能发生加成、取代、消去和缩聚反应 | |
| C. | 1mol对羟苯丙酮酸最多可与5molH2反应 | |
| D. | 1mol尿黑酸最多可与3molBr2反应 |
14.某同学在实验室探究NaHCO3的性质:常温下,配制0.10mol/LNaHCO3溶液,测其pH为8.4;取少量该溶液滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出.下列说法不正确的是( )
| A. | NaHCO3溶液呈碱性的原因是HCO3-的水解程度大于电离程度 | |
| B. | 加入CaCl2促进了HCO3-的水解 | |
| C. | 反应的离子方程式是2HCO3-+Ca2+═CaCO3↓+H2CO3 | |
| D. | 反应后的溶液中存在:c(Na+)+2c(Ca2+)═c(HCO3-)+2c(CO32-)+c(Cl-) |
1.下列实验中,现象和对应结论均正确的是( )
| 选项 | 实 验 | 现 象 | 结 论 |
| A | T℃时,向NaCl和NaBr的混合溶液中滴加AgNO3溶液 | 先出现白色沉淀 | T℃时,Ksp: AgCl<AgBr |
| B | 向等浓度的Na2CO3溶液或Na2SO4溶液中滴加酚酞试剂 | Na2CO3溶液变红色Na2SO4溶液无明显现象 | 非金属性:S>C |
| C | 常温下,取饱和CaSO4溶液或氨水做导电性实验 | 氨水实验的灯泡较亮 | CaSO4和NH3•H2O均为弱电解质 |
| D | 向品红溶液中滴加NaClO溶液或通入SO2气体 | 品红溶液均褪为无色 | 两者均有漂白性且 原理相同 |
| A. | A | B. | B | C. | C | D. | D |
18.通过溶解、过滤、蒸发等操作,可以将下列各组固体混合物分离的是( )
| A. | 硝酸钠 氢氧化钠 | B. | 氧化铜 二氧化锰 | ||
| C. | 氯化钾 碳酸钙 | D. | 硫酸铜 氢氧化钠 |