题目内容
在1L含0.001mol/LSO42-的溶液中加入0.01molBaCl2,能否使SO42-完全沉淀?此时SO42-的浓度是多少?(Ksp=1.08×10-10)
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:根据方程式计算可知氯化钡过量,根据Ksp和溶液中剩余的钡离子的浓度求出溶液中硫酸根离子的浓度.
解答:
解:发生反应的离子方程式为:Ba2++SO42-=BaSO4↓,已知n(SO42-)=0.001mol,n(Ba2+)=0.01mol,则钡离子过量,
剩余的钡离子浓度为c(Ba2+)=
=0.009mol/L,则c(SO42-)=
=
=1.2×10-8mol/L,所以能使SO42-完全沉淀,
答:能使SO42-完全沉淀,此时SO42-的浓度是1.2×10-8mol/L.
剩余的钡离子浓度为c(Ba2+)=
| 0.01mol-0.001mol |
| 1L |
| Ksp |
| c(Ba2+) |
| 1.08×10-10 |
| 0.009 |
答:能使SO42-完全沉淀,此时SO42-的浓度是1.2×10-8mol/L.
点评:本题考查了溶液中离子浓度的计算、溶度积常数的应用,侧重于考查学生的计算能力,题目难度中等.

练习册系列答案
相关题目
下列各组物质按酸、碱、单质、氧化物顺序排列的是( )
| A、H2SO4 Na2O C CO |
| B、Mg(OH)2 CuSO4 C CO2 |
| C、KOH HNO3 O2 SO3 |
| D、HCl NaOH O2 P2O5 |
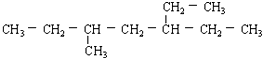 含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )
含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )| A、4种 | B、5种 | C、6种 | D、7种 |





 ;
;
