题目内容
(12分)有一包含有碳酸钠杂质的碳酸氢钠样品。为了测定其纯度,某校同学在实验室进行如下实验。甲组实验方案:
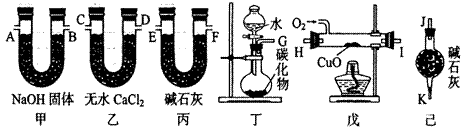
在坩埚中称取样品3.0g →加热→冷却→称量→再加热?…(至恒重)。
①完成上述实验应该用到的玻璃仪器除酒精灯外还有____ ____。
②若坩埚质量为16.0g,加热至恒重时坩埚和残留物总质量为18.2g,则样品的纯度为 _
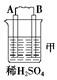
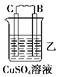
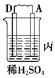
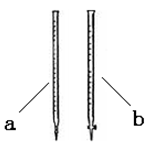
(1)乙组:称取样品,利用下面的部分装置测得室温下样品与酸反应放出CO2的体积,计算样品的纯度(已知碳酸钠、碳酸氢钠与酸的反应都是放热反应)。
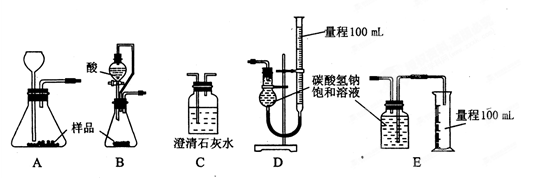
①完成该实验方案应选择的最佳装置是 __(用字母回答,下同)。
②该实验应选用的酸是_ _
a.稀盐酸b.稀硫酸c.稀硝酸d.三种酸均可。理由是________________________
(2) 丙组中A同学根据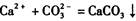 的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
B同学对该实验方案提出质疑,丙组同学查阅了相关资料,并进行了如下实验:
室温下,取20 mL0.4 mol/L NaHCO3溶液置于烧杯中,向其中加入20 mL 2 mol/L CaCl2溶液,用玻璃棒搅拌。烧杯中出现白色沉淀,还有气泡产生。产生该现象的原因是_________ __ ___ (用有关离子方程式解释)。
由此丙组同学共同讨论,否定了A同学的设计方案。
在坩埚中称取样品3.0g →加热→冷却→称量→再加热?…(至恒重)。
①完成上述实验应该用到的玻璃仪器除酒精灯外还有____ ____。
②若坩埚质量为16.0g,加热至恒重时坩埚和残留物总质量为18.2g,则样品的纯度为 _
(1)乙组:称取样品,利用下面的部分装置测得室温下样品与酸反应放出CO2的体积,计算样品的纯度(已知碳酸钠、碳酸氢钠与酸的反应都是放热反应)。

①完成该实验方案应选择的最佳装置是 __(用字母回答,下同)。
②该实验应选用的酸是_ _
a.稀盐酸b.稀硫酸c.稀硝酸d.三种酸均可。理由是________________________
(2) 丙组中A同学根据
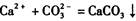 的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。B同学对该实验方案提出质疑,丙组同学查阅了相关资料,并进行了如下实验:
室温下,取20 mL0.4 mol/L NaHCO3溶液置于烧杯中,向其中加入20 mL 2 mol/L CaCl2溶液,用玻璃棒搅拌。烧杯中出现白色沉淀,还有气泡产生。产生该现象的原因是_________ __ ___ (用有关离子方程式解释)。
由此丙组同学共同讨论,否定了A同学的设计方案。

甲组实验方案:
①完成上述实验应该用到的玻璃仪器除酒精灯外还有玻璃棒、干燥器
②若坩埚质量为16.0g,加热至恒重时坩埚和残留物总质量为18.2g,,加热后固体质量为18.2g,-16.0g=2.2g 样品减少的质量为3.0g-2.2g=0.8g
固体减少的质量是碳酸氢钠分解生成水蒸气和二氧化碳的质量。根据质量差求出碳酸氢钠的质量=(168×0.8)/62=2.17g 则样品的纯度为2.17g/3.0g=72.3%
(1)乙组:①完成该实验方案应选择的最佳装置是B D
②该实验应选用的酸是稀硫酸,选b,因为硫酸没有挥发性
(2) 丙组:产生该现象的原因用离子方程式表示为Ca2++2HCO3-=CaCO3↓+CO2↑+H2O
①完成上述实验应该用到的玻璃仪器除酒精灯外还有玻璃棒、干燥器
②若坩埚质量为16.0g,加热至恒重时坩埚和残留物总质量为18.2g,,加热后固体质量为18.2g,-16.0g=2.2g 样品减少的质量为3.0g-2.2g=0.8g
固体减少的质量是碳酸氢钠分解生成水蒸气和二氧化碳的质量。根据质量差求出碳酸氢钠的质量=(168×0.8)/62=2.17g 则样品的纯度为2.17g/3.0g=72.3%
(1)乙组:①完成该实验方案应选择的最佳装置是B D
②该实验应选用的酸是稀硫酸,选b,因为硫酸没有挥发性
(2) 丙组:产生该现象的原因用离子方程式表示为Ca2++2HCO3-=CaCO3↓+CO2↑+H2O

练习册系列答案
相关题目
 NaCl杂质,为测
NaCl杂质,为测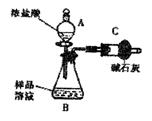
 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)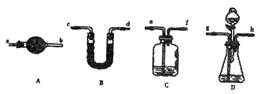
 烯中碳、氢两种元素的质量比。
烯中碳、氢两种元素的质量比。