题目内容
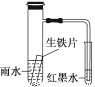
下图小试管内为红墨水,具支试管内盛有pH=4久置的雨水和生铁片。实验观察到:开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管内液面。下列说法正确的是
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水回升时,碳电极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液酸性增强
C
【解析】
试题分析:正常雨水的pH是5.6,溶液呈酸性,生铁中含有碳和铁,酸性条件下,生铁发生析氢腐蚀生成氢气,导致具支试管内气体压强大于大气压,导管内液面下降,当溶液呈弱酸性或中性时,生铁发生吸氧腐蚀,导致具支试管中气体压强小于大气压,导管内液面回升,略高于小试管液面。所以A.生铁片中的碳是原电池的正极,发生还原反应,铁是负极,发生氧化反应,错误;B.雨水酸性较强,开始时生铁片发生析氢腐蚀,一段时间后酸性减弱发生吸氧腐蚀,错误;C.墨水回升时,生铁发生吸氧腐蚀,碳电极是原电池的正极,反应式为O2+2H2O+4e-===4OH-,正确;D.先发生析氢腐蚀,消耗氢离子,后发生吸氧腐蚀,产生氢氧根离子,具支试管中溶液pH逐渐增大,酸性减弱,错误;
考点:考查金属的电化学腐蚀。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是
Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是 2C(g),
2C(g), O2(g)===FeO(s) ΔH1=-272 kJ/mol
O2(g)===FeO(s) ΔH1=-272 kJ/mol O2(g)===Al2O3(s) ΔH2=-1 675 kJ/mol
O2(g)===Al2O3(s) ΔH2=-1 675 kJ/mol
 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: