题目内容
下列基态原子的电子排布式中,其未成对电子数最多的是( )
| A、1s22s22p63s23p63d64s2 |
| B、1s22s22p63s23p64s1 |
| C、1s22s22p63s23p63d54s1 |
| D、1s22s22p63s23p63d104s1 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据各个原子中未成对电子个数判断,当原子中每个能级上电子处于半满时,该能级中未成对电子数最多,据此分析解答.
解答:
解:A.1s22s22p63s23p63d64s2中未成对电子数是4;
B.1s22s22p63s23p64s1中未成对电子数是5;
C.1s22s22p63s23p63d54s1中未成对电子数是6;
D.1s22s22p63s23p63d104s1中未成对电子数是1;
通过以上分析知,原子中未成对电子数最多的是C,
故选C.
B.1s22s22p63s23p64s1中未成对电子数是5;
C.1s22s22p63s23p63d54s1中未成对电子数是6;
D.1s22s22p63s23p63d104s1中未成对电子数是1;
通过以上分析知,原子中未成对电子数最多的是C,
故选C.
点评:本题考查了原子核外电子排布,明确原子核外电子排布规律是解本题关键,知道原子核外电子能量大小规律,知道原子轨道中电子处于半满、全满或全空时该原子最稳定,原子核外电子排布中常考查的原子有Cr、Cu.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列化合物中,既有离子键,又有共价键的是( )
| A、CaO |
| B、SiO2 |
| C、H2O |
| D、Na2O2 |
NA表示阿伏加德罗常数的值,下列说法一定正确的是( )
| A、7.8g Na2S和Na2O2的混合物中含有的离子总数为0.3NA |
| B、将1mol KClO3和SO3的混合物溶于水,溶液中自由移动的离子数目为3NA |
| C、标准状况下,22.4L氯气与足量的铁反应,转移电子数为0.2 NA |
| D、常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1 NA |
能正确表示下列化学反应的离子方程式的是( )
| A、氢氧化钡溶液与硫酸的反应:OH-+H+=H2O |
| B、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、二氧化碳与足量的氢氧化钠反应:CO2+2OH-=CO32-+H2O |
下列关于价电子构型为3s23p4的粒子描述正确的是( )
| A、它的原子核外有三种形状不同的电子云 |
| B、它的原子核外电子共有16种不同的运动状态 |
| C、它可与H2反应生成的化合物为非极性分子 |
D、核外电子轨道表示式为: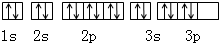 |
下列有机反应中,不属于取代反应的是( )
A、 CH3+Cl2 CH3+Cl2
 CH2Cl+HCl CH2Cl+HCl | |||
B、2CH3CH2OH+O2
| |||
| C、CH2=CH2+Cl2→一定条件 CH2=CHCl+HCl | |||
D、ClCH2CH=CH2+NaOH
|