题目内容
10.有一种有机物结构简式为:HOCH2-CH=CHCH2COOCH2CH3,推测它不可能具有下列哪种性质( )| A. | 常温下,能被酸性高锰酸钾溶液氧化 | |
| B. | 该分子最少有4个碳原子共平面 | |
| C. | 常温下,能在碱性条件下发生水解反应 | |
| D. | 常温下,能够与碳酸钠溶液反应生成CO2 |
分析 HOCH2-CH=CHCH2COOCH2CH3中含有酯基,可发生水解反应;含有碳碳双键,可发生加成、加聚和氧化反应,含有羟基,可发生取代、氧化反应,以此解答该题.
解答 解:A.含有羟基、碳碳双键,可被酸性高锰酸钾氧化,故A不选;
B.碳碳双键具有平面形结构,与碳碳双键直接相连的原子在同一个平面上,则该分子最少有4个碳原子共平面,故B不选;
C.含有酯基,可在碱性条件下发生水解反应,故C不选;
D.不含羧基,与碳酸钠不反应,故D选.
故选D.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力和有机物知识的综合运用,难度不大,注意把握有机物的官能团的性质,为解答该题的关键.

练习册系列答案
相关题目
1. 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g).如图是A的反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g).如图是A的反应速率v(A)随时间变化的示意图.下列说法正确的是( )
 在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g).如图是A的反应速率v(A)随时间变化的示意图.下列说法正确的是( )
在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)?3C(g).如图是A的反应速率v(A)随时间变化的示意图.下列说法正确的是( )| A. | 反应物A的浓度:a点小于b点 | |
| B. | 该反应的某种生成物可能对反应起催化作用 | |
| C. | 曲线上的c、d两点都表示达到平衡状态 | |
| D. | A的平均反应速率:ab段大于bc段 |
15.某原电池的总反应离子方程式为:2Fe3+十Fe═3Fe2+,能实现该反应的原电池是( )
| 正 极 | 负 极 | 电解质溶液 | |
| A | Cu | Fe | FeCl3 |
| B | C | Fe | Fe(NO3)3 |
| C | Fe | Zn | Fe2(SO4)3 |
| D | Ag | Fe | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
19.某有机物M的结构简式为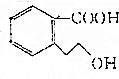 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )
 ,下列有关M的说法正确的是( )
,下列有关M的说法正确的是( )| A. | M的分子式为C9H10O3 | |
| B. | M 可使酸性KMnO4溶液褪色 | |
| C. | 1 mol M完全燃烧消耗10 mol O2 | |
| D. | 1 mol M能与足量Na反应生成0.5 mol H2 |
20.已知CO(g)+H2O(g)?CO2(g)+H2(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
 ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025a kJ•mol-1
;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:SiCl4(g)+2H2(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025a kJ•mol-1