题目内容
 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )①Zn是负极
②电子由Zn经外电路流向Cu
③负极反应为Zn-2e-=Zn2+
④H+在溶液中向Cu棒迁移,SO42-向Zn棒迁移.
| A、只有①② | B、只有①②③ |
| C、只有②③④ | D、①②③④ |
考点:原电池和电解池的工作原理
专题:
分析:锌、铜和稀硫酸组成的原电池中,活泼性较强的锌为原电池的负极,发生:Zn-2e-=Zn2+而被氧化,原电池工作时,电子由负极经外电路流向正极,电解质溶液中,H+流向正极,在Cu棒上得电子被还原为氢气,以此解答该题.
解答:
解:①锌、铜和稀硫酸组成的原电池中,活泼性较强的锌为原电池的负极,故①正确;
②原电池工作时,电子由负极经外电路流向正极,即电子由Zn经外电路流向Cu,故②正确;
③锌为原电池的负极,发生:Zn-2e-=Zn2+而被氧化,故③正确;
④电解质溶液中,H+流向正极在Cu棒,SO42-向负极Zn棒迁移,故④正确;
故选D.
②原电池工作时,电子由负极经外电路流向正极,即电子由Zn经外电路流向Cu,故②正确;
③锌为原电池的负极,发生:Zn-2e-=Zn2+而被氧化,故③正确;
④电解质溶液中,H+流向正极在Cu棒,SO42-向负极Zn棒迁移,故④正确;
故选D.
点评:本题考查原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意把握电解方程式的书写,难度不大.

练习册系列答案
相关题目
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )

| A、X可能是一种氢化物 |
| B、M可能是金属 |
| C、E可能是一种有色气体 |
| D、F浓溶液能使某些金属钝化 |
短周期元素A、B、C、D、E.已知A、B为金属,C、D、E为非金属,C是最活泼的非金属,E与C同主族,D离子半径比E离子半径大,A、B的离子与C离子电子层结构相同,其中B离子的半径最小,.下列有关说法错误的是( )
| A、含氧酸的酸性:E>D |
| B、原子半径:A>B |
| C、氢化物的热稳定性:C>E |
| D、离子结合成质子能力:D>E |
下列说法正确的是( )
| A、葡萄糖与淀粉互为同分异构体 |
| B、糖类、油脂、蛋白质都是高分子化合物 |
| C、糖类、油脂、蛋白质都能发生水解 |
| D、油脂有油和脂肪之分,但都属于酯 |
化学与生活密不可分,下列关于物质的用途的叙述不正确的是( )
| A、碳酸氢钠可用于焙制糕点 |
| B、氨在常压冷却或常温加压的条件下可以液化为无色液体液氨,液氨的用途之一是用作生活中的制冷剂 |
| C、碳酸钡难溶于水和酸,可做X光透视胃的药剂 |
| D、每年春节全国各地齐放焰火充满新年气氛,这主要利用了化学中“焰色反应”的知识 |
对下列事实的解释错误的是( )
| A、在蔗糖中加入浓硫酸后出现黑色物质,说明浓硫酸具有脱水性 |
| B、浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C、常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 |
| D、干燥的氯气通入干燥的红色纸条中不褪色,说明氯气本身没有漂白性 |
有机物A的结构简式为 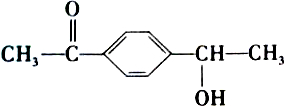 ,有关它的说法正确的是( )
,有关它的说法正确的是( )
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A、A遇FeCl3溶液显紫色 |
| B、A被酸性KMnO4溶液氧化可生成羧酸 |
| C、乙酸与A形成的酯的化学式是C12H14O3 |
| D、A能发生取代、加成、消去、氧化、聚合等反应 |
下列各组元素中按微粒半径递增顺序排列的是( )
| A、K、Na、Li |
| B、Ba2+、Ca2+、Mg2+? |
| C、N、O、F |
| D、Ca2+、K+、Cl- |