题目内容
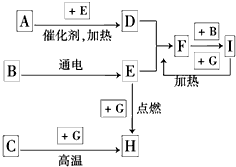
如图是中学化学中常见物质间的反应转化关系图,其中部分产物已略去.常温下,G为固体单质,B、I为液体,其余都为气体.A为化合物,I的浓溶液与G在加热条件下生成F、B和C.H可用作工业冶炼金属的还原剂.请按要求填空:
(1)写出下列物质的化学式:
A. ,B. ,C. .
(2)写出A→D的化学方程式: .
(3)写出G和I的浓溶液反应的化学方程式: .
(4)工业上制I的尾气中通常混有D和F,D和F都是大气污染物,工业上通常用苛性钠溶液来吸收尾气中的D和F,请写出相关的化学方程式: 、 ;要使D和F被完全吸收,其物质的量关系必须满足: ,为达到这个要求,可以向尾气中通入一定量的 来调节D和F的物质的量关系.

(1)写出下列物质的化学式:
A.
(2)写出A→D的化学方程式:
(3)写出G和I的浓溶液反应的化学方程式:
(4)工业上制I的尾气中通常混有D和F,D和F都是大气污染物,工业上通常用苛性钠溶液来吸收尾气中的D和F,请写出相关的化学方程式:
考点:无机物的推断
专题:
分析:气体H可用作工业冶炼金属的还原剂,推断H为CO,所以G为碳,C为CO2,E与G点燃得到H,则E为O2,液体B电解得到氧气,故B为H2O,G和I浓溶液反应得到水、气体F与C,而F与水反应又得到I,则I为HNO3,F为NO2,可推知D为NO,A为NH3,验证符合转化关系,据此解答.
解答:
解:气体H可用作工业冶炼金属的还原剂,推断H为CO,所以G为碳,C为CO2,E与G点燃得到H,则E为O2,液体B电解得到氧气,故B为H2O,G和I浓溶液反应得到水、气体F与C,而F与水反应又得到I,则I为HNO3,F为NO2,可推知D为NO,A为NH3,验证符合转化关系,
(1)由上述分析可知,A为NH3,B为H2O,C为CO2,故答案为:NH3;H2O;CO2;
(2)A为NH3,分子结构为三角锥形,故答案为:三角锥;
(3)A→D是NH3在催化剂作用下加热和氧气反应生成一氧化氮和水,反应的化学方程式:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
(4)G和I的浓溶液反应是碳单质和浓硝酸加热反应生成二氧化碳、二氧化氮和水,反应的化学方程式为:C+4HNO3(浓)
CO2↑+2H2O+4NO2↑,
故答案为:C+4HNO3(浓)
CO2↑+2H2O+4NO2↑;
(5)用苛性钠溶液来吸收尾气中的NO和NO2,相关的化学方程式为:NO2+NO+2NaOH═2NaNO2+H2O、2NO2+2NaOH═NaNO3+NaNO2+H2O,由方程式可知,只有二氧化氮可以被吸收、二氧化氮与NO按1:1混合可以被完全吸收,要使NO和NO2被完全吸收,应满足:n(NO2)≥n(NO),为达到这个要求,可以向尾气中通入一定量的空气来调节NO和NO2的物质的量关系,
故答案为:NO2+NO+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO3+NaNO2+H2O;n(NO2)≥n(NO);空气.
(1)由上述分析可知,A为NH3,B为H2O,C为CO2,故答案为:NH3;H2O;CO2;
(2)A为NH3,分子结构为三角锥形,故答案为:三角锥;
(3)A→D是NH3在催化剂作用下加热和氧气反应生成一氧化氮和水,反应的化学方程式:4NH3+5O2
| ||
| △ |
| ||
| △ |
(4)G和I的浓溶液反应是碳单质和浓硝酸加热反应生成二氧化碳、二氧化氮和水,反应的化学方程式为:C+4HNO3(浓)
| ||
故答案为:C+4HNO3(浓)
| ||
(5)用苛性钠溶液来吸收尾气中的NO和NO2,相关的化学方程式为:NO2+NO+2NaOH═2NaNO2+H2O、2NO2+2NaOH═NaNO3+NaNO2+H2O,由方程式可知,只有二氧化氮可以被吸收、二氧化氮与NO按1:1混合可以被完全吸收,要使NO和NO2被完全吸收,应满足:n(NO2)≥n(NO),为达到这个要求,可以向尾气中通入一定量的空气来调节NO和NO2的物质的量关系,
故答案为:NO2+NO+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO3+NaNO2+H2O;n(NO2)≥n(NO);空气.
点评:本题考查无机物推断,H可用作工业冶炼金属的还原剂、物质的状态、转化中特殊反应等是推断突破口,需要学生熟练掌握元素化合物性质,难度中等.

练习册系列答案
相关题目
下列关于能源的开发和利用的说法中不正确的是( )
| A、能源是有限的,无节制地利用常规能源,是一种盲目的短期行为 |
| B、根据能量守恒定律,担心能源枯竭是杞人忧天 |
| C、在能源的开发和利用中必须同时考虑对环境的影响 |
| D、人类的生存离不开能源,社会的进步和美好生活是以消耗大量能源为代价的,我们要珍惜能源 |
下列说法中正确的是( )
| A、物质的量浓度和体积相同的K2CO3、K2SO4、HCl溶液混合后,溶液的pH<7 | ||
| B、NH4HSO4稀溶液中,c(SO42-)>c(NH4+)>c(H+)>c(OH -) | ||
C、将0.1mol/L的CH3COOH溶液加水稀释,溶液中的
| ||
| D、t℃时,某稀Ba(OH)2溶液中c(H+)?c(OH -)=1.0×10-12.向pH=8的该溶液中加入等体积pH=4的盐酸,则混合后溶液pH=6 |
在40GPa的高压下,用激光加热到1800K,成功的制得了原子晶体CO2,下列有关该物质的推断正确的是( )???
| A、该原子晶体中含有CO2分子 |
| B、该原子晶体易汽化,可用作制冷材料 |
| C、该原子晶体质软,可切割 |
| D、该原子晶体有很高的熔、沸点 |
向硝酸钠溶液中加入铜粉不发生反应,再加入某种盐,铜粉可以逐渐溶解,符合条件的盐( )
| A、ZnSO4 |
| B、NaHCO3 |
| C、NaHSO4 |
| D、Fe(NO3)3 |
 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F均用所对应的元素符号表示):
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F均用所对应的元素符号表示):
