题目内容
向硝酸钠溶液中加入铜粉不发生反应,再加入某种盐,铜粉可以逐渐溶解,符合条件的盐( )
| A、ZnSO4 |
| B、NaHCO3 |
| C、NaHSO4 |
| D、Fe(NO3)3 |
考点:硝酸的化学性质
专题:
分析:硝酸盐在酸性条件下具有硝酸的强氧化性,则可使Cu溶解;铜具有还原性,遇强氧化性物质可以发生氧化还原反应,据此来解答也可.
解答:
解:A、Cu、NaNO3、ZnSO4混合时不反应,故A不选;
B、碳酸氢钠为弱酸盐,水解显碱性,不能提供酸性环境,不能反应,故B不选;
C、Cu、NaNO3混合时加入NaHSO4,硫酸氢钠电离出氢离子,发生3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,则铜粉质量减轻,故C选;
D、硝酸铁与铜反应氧化还原反应,可以溶解,故D选;
故选CD.
B、碳酸氢钠为弱酸盐,水解显碱性,不能提供酸性环境,不能反应,故B不选;
C、Cu、NaNO3混合时加入NaHSO4,硫酸氢钠电离出氢离子,发生3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,则铜粉质量减轻,故C选;
D、硝酸铁与铜反应氧化还原反应,可以溶解,故D选;
故选CD.
点评:本题考查硝酸盐在酸性条件下的性质,明确选项中各物质的性质及发生的化学反应是解答本题的关键,难度不大.

练习册系列答案
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
已知17X、34Y、35Z三种原子,据其在周期表中的位置,判断下列说法正确的是( )
| A、原子半径:X>Y>Z |
| B、气态氢化物的稳定性Y>X>Z |
| C、单质熔点:Y>X>Z |
| D、简单阴离子的还原性:Y>Z>X |
化学与生活密不可分,下列关于物质的用途的叙述不正确的是( )
| A、碳酸氢钠可用于焙制糕点 |
| B、氨在常压冷却或常温加压的条件下可以液化为无色液体液氨,液氨的用途之一是用作生活中的制冷剂 |
| C、碳酸钡难溶于水和酸,可做X光透视胃的药剂 |
| D、每年春节全国各地齐放焰火充满新年气氛,这主要利用了化学中“焰色反应”的知识 |
大理石是一种重要的化工原料,其主要成分可以反应生成一系列物质,如下图所示.
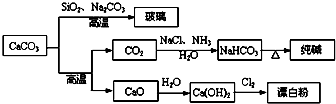
下列说法正确的是( )

下列说法正确的是( )
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、向饱和碳酸钠溶液中通入过量CO2,溶液变浑浊 | ||||
| D、制取玻璃和漂白粉所涉及的反应都是非氧化还原反应 |
天然气和液化石油气(主要成分为C3~C5的烷烃)燃烧的化学方程式分别为:CH4+2O2
CO2+2H2O,C3H8+5O2
CO2+4H2O,现有一套以天然气为燃料的灶具,今改用液化石油气,应采取的正确措施是( )
| 点燃 |
| 点燃 |
| A、增大空气进入量或减小石油气进入量 |
| B、增大空气进入量或增大石油气进入量 |
| C、减小空气进入量或减小石油气进入量 |
| D、减小空气进入量或增大石油气进入量 |
下列变化中,不需要破坏化学键的是( )
| A、加热氯化铵使其分解 |
| B、氯化钠晶体熔化 |
| C、干冰气化 |
| D、氯化氢溶于水 |
下列有关氢化物的叙述中正确的是( )
| A、稳定性:HF>H2S>H2O |
| B、沸点:H2O>NH3>PH3 |
| C、一个D2O分子中所含的中子数为12 |
| D、在卤化氢中HF的还原性最强 |